
Traduit en Français par François Mériaux (fm@osteo-animalier.com)
https://doi.org/10.32388/S6IGL0
Résumé
L’Impulsion Rythmique Crânienne (IRC), ou Mécanisme Respiratoire Primaire (MRP), un rythme perçu par les ostéopathes à la surface de la peau, est un concept fondamental que certains d’entre eux utilisent dans leur pratique pour leur diagnostic et leur traitement.
Cependant, la base physiologique de ce phénomène reste flou.
Sutherland, fondateur de l’ostéopathie crânienne, a proposé en 1939 une théorie qui est restée dogmatique, malgré les avancées scientifiques qui l’ont réfutée.
Depuis 1990, certains ostéopathes ont essayé de trouver de meilleures explications, comme celles présentées dans une précédente revue systématique [1].
Dans cette revue narrative, nous revenons d’abord sur chaque pilier de la théorie de Sutherland, en les analysant à la lumière des études scientifiques les plus récentes afin d’évaluer si la recherche contemporaine soutient ou remet en question ses idées.
Après avoir montré que ce modèle est incohérent avec les données actuelles de la science, nous explorons les connaissances scientifiques sur les mécanismes physiologiques sous-jacents au MRP/IRC.
L’hypothèse la plus plausible pour expliquer cela repose sur la variation de la matrice extracellulaire et de la texture fasciale, influencée par les oscillations rythmiques de la pression sanguine (ondes de Traube Hering et Mayer), et par l’interaction d’autres rythmes physiologiques (ventilation, baroréflexe, variabilité de la fréquence cardiaque…).
Enfin, nous discutons de la pertinence et des applications pratiques du MRP en ostéopathie.
Tandis que le modèle de Sutherland continue de prévaloir dans les croyances dominantes, la littérature scientifique a mis de plus en plus l’accent sur l’activité du système autonome comme hypothèse principale.
Cette analyse narrative souligne la nécessité d’un changement de paradigme concernant l’IRC/MRP en ostéopathie, en plaidant pour une communication plus claire d’un modèle aligné sur les données scientifiques les plus récentes.
Introduction
Le terme Mécanisme Respiratoire Primaire (MRP) est couramment utilisé par certains ostéopathes pour décrire la sensation palpatoire d’un rythme physiologique à la surface de la peau [1].
Il peut être utilisé pour leur diagnostic et leur traitement.
Il est décrit comme ayant deux phases, une phase d’expansion (inspiration) et une phase de contraction (expiration) [2][3].
Il est différent de la respiration puisqu’il reste perceptible lorsque le patient retient sa respiration [4].
Historiquement, l’ostéopathe qui l’a décrit en premier, William Garner Sutherland (1873-1954), a eu l’intuition que les sutures crâniennes étaient faites pour le mouvement et a imaginé un modèle basé sur cinq principes : la mobilité inhérente du système nerveux central et de la moelle épinière ; la fluctuation du liquide céphalo-rachidien (LCR) ; les membranes de tension réciproque ; la mobilité articulaire des os du crâne ; le mouvement involontaire du sacrum entre les os iliaques [2][3].
Sutherland a choisi le terme « Mécanisme Respiratoire Primaire » (MRP) pour mettre en évidence plusieurs aspects clés de son concept.
Le mot mécanisme indique que le MRP est un phénomène physiologique organisé, où plusieurs éléments interagissent de manière coordonnée.
Le terme respiratoire a été choisi par analogie avec la respiration pulmonaire, mais il se réfère à un processus différent.
Pour Sutherland, le MRP représentait une pulsation rythmique autonome dans le corps, essentielle à la vie et présente même en l’absence de respiration pulmonaire [2].
Il voulait souligner que le corps possède un mouvement périodique interne, indépendant des poumons, animant les tissus et les fluides.
Le mot primaire signifie que ce mécanisme serait présent dès le début de la vie embryonnaire et constituerait une fonction vitale fondamentale.
De nombreux ostéopathes utilisent aujourd’hui le terme MRP pour décrire les micromouvements avec lesquels ils travaillent. À noter qu’en France, un glissement sémantique est observé : de nombreux ostéopathes utilisent le terme « mouvement » plutôt que « mécanisme » lorsqu’ils font référence au MRP.
Cependant, pour être précis et rester fidèle à son sens d’origine, le terme Impulsion Rythmique Crânienne (IRC) devrait être utilisé lorsqu’on fait spécifiquement référence à la sensation palpatoire de ce rythme à la surface de la peau.
Cette terminologie a été introduite en 1961 par Woods et Woods, qui ont perçu un rythme à la surface de la tête.
Ils l’ont relié au MRP de Sutherland et ont tenté, sept ans après sa mort, de définir une plage de fréquence normale, ce que Sutherland lui-même n’avait jamais fait [5].
Pour certains ostéopathes, l’IRC et le MRP représentent le même mouvement, ressenti respectivement au niveau du cuir chevelu et dans le reste du corps.
La confusion entre ces deux termes est fréquente [6], sans être problématique dans la mesure où l’IRC est généralement considérée comme une manifestation du MRP, cette assimilation relevant ainsi essentiellement d’une simplification.
Le MRP reste l’explication historique de ce rythme particulier, qui est l’objet de cette revue [7][8].
Les cinq phénomènes sous-jacents au MRP ont été décrits pour la première fois par Sutherland dans The Cranial Bowl (1939) et ont ensuite été largement diffusés par son élève Harold Magoun, qui a publié Osteopathy in the Cranial Field en 1951.
Magoun a ensuite cherché à structurer les enseignements de Sutherland, en les rendant plus accessibles et reproductibles par la formalisation de techniques et de protocoles [2][3].
Cependant, Sutherland était quelque peu réticent à cette formalisation biomécanique, craignant qu’elle ne limite une compréhension plus profonde de son approche.
Alors qu’il considérait le mouvement crânien comme un processus holistique influencé par de multiples facteurs, Magoun, dans son effort de popularisation de ces idées, risquait de réduire cette complexité à un ensemble prédéfini de pratiques, en décrivant des mouvements et des techniques spécifiques.
Cette divergence a créé certaines tensions, Sutherland craignant que l’essence de son travail ne soit perdue [2][3].
Néanmoins, tel est l’héritage dont nous disposons aujourd’hui : les ostéopathes perçoivent un rythme supposé être associé aux mouvements des os du crâne et à d’autres phénomènes, et c’est précisément cette hypothèse que nous cherchons à réévaluer.
Avec ces clarifications à l’esprit, nous avons choisi d’associer systématiquement les termes MRP et IRC afin de nous aligner sur l’usage courant, en faisant référence au rythme typique perçu par les ostéopathes.
Le MRP/IRC est défini par ses trois composantes : amplitude, rythme et force.
Si ces trois composantes sont correctes, l’ostéopathe peut conclure que le patient, ou au moins la zone sur laquelle il se concentre, est bien équilibré.
Certains ostéopathes pensent que le MRP/IRC peut être utilisé comme un outil pour vérifier l’efficacité de chaque traitement ostéopathique, en le contrôlant après chaque technique appliquée jusqu’à ce qu’il soit suffisamment bon pour marquer la fin de la séance.
Le MRP/IRC refléterait alors l’harmonie et la vitalité du corps.
L’amplitude devrait être large et symétrique.
La force est considérée comme correcte lorsqu’elle est perçue comme puissante.
Bien qu’en général le rythme soit considéré comme normal entre 6 et 12 cycles par minute (cpm), la littérature rapporte de grandes variations allant de 3 à 22 cpm [9].
La Figure 1 montre l’étendue des fréquences décrites dans la littérature, qui ne sont pas facilement attribuables à un rythme physiologique identifié.
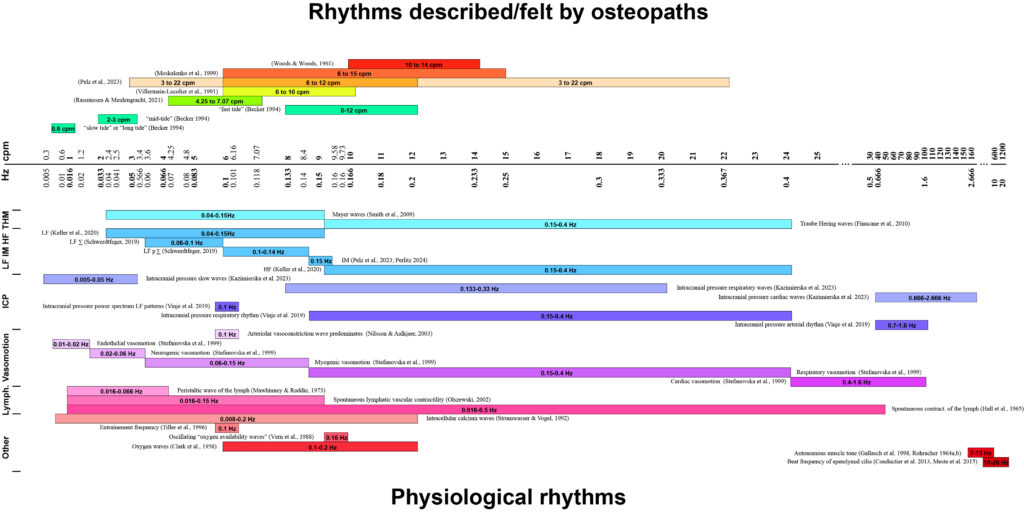
Figure 1. La présentation suivante exposera les différents rythmes et fréquences (exprimés en Hz et en cpm) décrits par les ostéopathes, en comparaison avec ceux des rythmes physiologiques. Ces rythmes seront regroupés dans les catégories suivantes : ondes de Traube Hering et Mayer (THM) ; basse fréquence (LF) ; fréquence intermédiaire (IM) ; haute fréquence (HF) ; onde de pression intracrânienne (ICP) ; vasomotion ; contractilité lymphatique spontanée (Lymph.) et autres. Pour Pelz et al. [8], l’intervalle de fréquence compris entre 3 et 22 Hz représente l’intervalle total des mesures, les intervalles plus restreints entre 6 et 12 Hz représentant la plage des valeurs les plus fréquemment retrouvées.
Ainsi, les différents rythmes perçus pourraient dépendre du couple praticien/patient et varier au cours du temps [10][11][12][2][13][14][15][5], rendant alors la mesure objective et la comparaison difficile, ce qui pourrait expliquer la faible reproductibilité intra- et inter-examinateur observée dans la littérature.
Par ailleurs, différentes études peuvent décrire des rythmes distincts sous une même terminologie.
Fait intéressant, des rythmes appartenant à la gamme de fréquence du MRP ont également été mis en évidence par des instruments de mesure, suggérant une possible objectivation du phénomène [10].
Dans une étude récente, Rasmussen et Meulengracht [4] ont démontré l’existence d’un troisième rythme physique (différent des rythmes cardiaque et respiratoire) détecté au niveau de la tête humaine par leur appareil, avec une moyenne de 6,16 cycles/minute (4,25–7,07).
Cependant, l’outil de mesure, bien que validé sur le plan métrologique dans leur laboratoire (Annexe A. Données supplémentaires dans [4]), présente un biais important, similaire à celui de l’outil utilisé par Frymann en 1971 : les mouvements de la tête générés par la ventilation ne sont pas contrôlables [16].
Nelson et al. [17][18][19][20], et plus récemment Pelz et al. [9], ont montré une corrélation statistiquement significative entre les mesures du flux sanguin cutané et la palpation de l’IRC, montrant que les manipulations crâniennes affectent ces paramètres objectifs.
Considérant l’existence d’études sérieuses suggérant que le MRP/IRC pourrait exister et qu’un praticien entraîné pourrait le percevoir, nous avons récemment réalisé une revue systématique structurée de la littérature dans MEDLINE, Science Direct et la Cochrane Library sur ce sujet afin de décrypter les différentes hypothèses des mécanismes physiologiques supposés sous-tendre le rythme MRP/IRC [1].
Cette revue systématique et la Figure 1 montrent que la question de la base physiologique de ce rythme reste controversée.
Le modèle initial proposé par Sutherland n’est plus compatible avec les connaissances physiologiques actuelles, et les mécanismes sous-jacents à ce phénomène restent incertains.
Les résultats de notre précédente revue systématique ont mis en évidence la nécessité d’un changement de paradigme et d’une évaluation et communication plus rigoureuses d’un modèle en accord avec l’évolution des données scientifiques.
C’est dans cette perspective que s’inscrit la présente revue narrative, qui intègre des données issues de différents domaines des sciences de la vie.
Après une première partie réaffirmant que le modèle de Sutherland n’est plus compatible avec les connaissances scientifiques actuelles, nous étudions les rôles poententiels de la vasomotion, du système nerveux autonome, de la microcirculation, du système lymphatique, de la matrice extracellulaire, du réseau fascial et des phénomènes d’entrainement dans la genèse du MRP/IRC. Sur cette base, nous proposons un modèle intégratif et soulignons la nécessité d’une évolution conceptuelle.
II. Méthodes
Cette revue a été menée conformément aux recommandations développées par Tricco et al. pour la réalisation d’une revue narrative suivant la déclaration PRISMA-AcR [21].
Le cadre théorique de cette revue de portée a été élaboré par une équipe de trois experts (F.M., L.S., A.G.) spécialisés en recherche scientifique (L.S., A.G.) et dans l’enseignement et la pratique clinique de l’ostéopathie (F.M., L.S.).
Le cadre présent est basé sur les résultats et conclusions de l’article de Mériaux et al. [1].
Question de recherche
Quelles sont les données scientifiques actuellement disponibles permettant de déterminer si les recherches contemporaines soutiennent ou remettent en question le modèle empirique du mécanisme respiratoire primaire (MRP) décrit par Sutherland [2][3] ?
Stratégie de recherche
Une recherche systématique de la littérature a été finalisée en octobre 2023 à partir des bases de données bibliographiques indexées MEDLINE, ScienceDirect et Cochrane Library [1]. Cette première recherche a permis d’identifier huit domaines de recherche susceptibles d’apporter des explications physiologiques complémentaires à l’IRC/MRP, au-delà des cinq piliers décrits par Sutherland : le système lymphatique, la vasomotricité, les ondes de Traube-Hering et de Mayer, la variabilité de la fréquence cardiaque, la fréquence ventilatoire, la matrice extracellulaire, les hypothèses métaboliques et l’embryologie.
Une recherche documentaire complémentaire et approfondie a ensuite été menée entre septembre 2024 et février 2025 à l’aide des bases PubMed, ScienceDirect, Ostmed.DR et Google Scholar. Les mots-clés ont été adaptés à chaque base de données : cranial rhythmic impulse ; primary respiratory mechanism ; Traube-Hering waves, Mayer waves ; cranial osteopathy ; osteopathy in the cranial field ; craniosacral therapy ; cranial osteopathic manipulative medicine ; heart rate variability ; cranial bone mobility ; central link ; vasomotion ; autonomic nervous system ; ventilation ; muscle tone ; microcirculation ; lymphatic system ; glymphatic systems ; extracellular matrix ; training ; embryological movement ; ideomotion ; intracranial pressure.
Aucune restriction n’a été appliquée concernant le type d’étude, la population étudiée, les critères de jugement ou la date de publication. Les articles ont d’abord été sélectionnés à partir de la lecture de leurs résumés afin d’en évaluer la pertinence, puis analysés dans leur intégralité. Les bibliographies des articles retenus ont également été examinées et une stratégie dite « boule de neige » (snowballing) a été utilisée afin d’identifier d’autres travaux pertinents.
Critères d’éligibilité
Afin de garantir une couverture aussi large que possible de la littérature disponible, aucune évaluation formelle de la qualité méthodologique des études incluses n’a été réalisée. Chaque article a en revanche fait l’objet d’une analyse critique de sa pertinence vis-à-vis de la question de recherche lors de réunions de discussion entre les auteurs (F.M., L.S., A.G.).
Les études sélectionnées ont été analysées dans le but d’identifier les mécanismes physiologiques susceptibles soit de soutenir, soit de remettre en question le modèle du MRP. Lorsqu’elles abordaient plusieurs thématiques, certaines études ont été intégrées dans plusieurs catégories d’analyse.
Synthèse et catégorisation des données
Au total, 157 articles ont été retenus et regroupés selon les thématiques suivantes :
- La motilité inhérente du système nerveux central et de la moelle épinière ;
- Les fluctuations du liquide céphalorachidien ;
- La motilité des membranes intracrâniennes et intrarachidiennes ;
- La mobilité articulaire des os du crâne ;
- Le mouvement involontaire du sacrum entre les os iliaques (« hypothèse du lien central ») ;
- L’IRC/MRP et la vasomotricité ;
- L’IRC/MRP et le système nerveux autonome (incluant les ondes de Traube-Hering-Mayer et la variabilité de la fréquence cardiaque) ;
- Le MRP, la microcirculation, le système lymphatique, la matrice extracellulaire et le réseau fascial ;
- Le MRP et les phénomènes d’entraînement (entrainment) ;
- Le MRP et les mouvements embryologiques.
Les articles ont été identifiés principalement selon une stratégie de type snowballing, à partir des références déjà incluses dans la revue systématique de Mériaux et al. [1], complétées par l’expertise des auteurs dans le domaine ainsi que par l’analyse des bibliographies des études sélectionnées.
Cadre d’interprétation
L’analyse de la littérature suggère que les cinq piliers décrits par Sutherland puis formalisés par Magoun pourraient correspondre à un modèle empirique qui n’est pas pleinement soutenu par les connaissances scientifiques actuelles. En revanche, plusieurs phénomènes physiologiques rythmiques — notamment la vasomotricité, la variabilité de la fréquence cardiaque, la microcirculation et les ondes de Traube-Hering-Mayer — apparaissent comme des candidats plausibles pour contribuer à l’élaboration d’un modèle explicatif davantage fondé sur les données scientifiques contemporaines.
III. Résultats : réévaluation de la théorie de Sutherland
Le modèle de Sutherland est solidement ancré dans la littérature.
Cependant, nous montrerons dans cette section que ce modèle ne s’aligne pas avec les connaissances scientifiques contemporaines.
III.1. La motilité inhérente du système nerveux central et de la moelle épinière
Depuis 1882, de nombreux anatomistes ont observé et décrit le mouvement continu et cyclique de la masse cérébrale et de la moelle, correspondant à une systole et une diastole, qui, selon Sutherland, pourrait agir comme une pompe hydraulique activant le liquide céphalo-rachidien (LCR) [12].
Par la suite, Harold Magoun [2], puis John Upledger [15], ont proposé une interprétation différente. Selon eux, ce serait la production rythmique du LCR par les plexus choroïdes qui mettrait l’encéphale en mouvement, et non l’inverse.
Selon le modèle du « pressurestat » d’Upledger, la sécrétion du LCR se ferait à une vitesse deux fois supérieure à sa résorption. Des mécanorécepteurs situés au niveau des sutures crâniennes détecteraient un seuil maximal de pression intracrânienne et, par un mécanisme de rétrocontrôle, interrompraient temporairement la sécrétion jusqu’à ce que la pression redescende. La production reprendrait alors, générant ainsi un cycle oscillatoire.
Cependant, ce modèle n’est pas compatible avec les connaissances actuelles. La production du LCR n’est ni intermittente ni rythmique [10]. Lorsque la pression intracrânienne augmente, la résorption du LCR augmente simultanément grâce à l’accroissement de la surface d’échange des villosités arachnoïdiennes au sein des sinus veineux. Cette description théorique est connue sous le nom de doctrine « statique » de Monro-Kellie [22][23].
Dans des conditions physiologiques, les volumes intracrâniens restent dans un état d’équilibre dynamique : toute augmentation du volume d’un compartiment (parenchyme cérébral, sang ou LCR) est compensée par une diminution d’un autre. Cette compensation n’est toutefois pas instantanée et génère des variations transitoires de pression intracrânienne (PIC) [24].
Ces variations de PIC sont d’une grande importance clinique et sont notamment surveillées chez les patients souffrant de traumatismes crâniens ou d’hydrocéphalie. Elles peuvent être enregistrées de manière non invasive à l’aide de capteurs mécaniques placés sur le cuir chevelu, capables de détecter les déformations micrométriques du crâne battement après battement [25–27]. Dès 1985, Pitlyk et al. avaient montré que ces faibles expansions crâniennes reflétaient les variations de pression intracrânienne [28].
Dans le domaine temporel, le signal de PIC est constitué de plusieurs composantes superposées. L’analyse fréquentielle permet toutefois de distinguer :
- les ondes lentes (0,3 à 3 cycles par minute) ;
- les ondes respiratoires (8 à 20 cycles par minute) ;
- les ondes cardiaques (40 à 160 cycles par minute) [29][24].
Vinje et al. [30] ont mesuré les gradients de pression intracrânienne à l’aide de deux capteurs implantés simultanément. Leur analyse spectrale a mis en évidence deux pics principaux : l’un correspondant au rythme artériel (0,7 à 1,6 Hz ; 42 à 96 battements/minute), l’autre à l’activité respiratoire (0,15 à 0,4 Hz ; 9 à 24 respirations/minute). Fait intéressant, ils ont également observé des oscillations de basse fréquence inférieures à 0,1 Hz (environ 6 cycles/minute), sans toutefois évaluer leur contribution au flux du LCR [30].
En utilisant l’imagerie par résonance magnétique (IRM), Maier et al. [13] ont déjà observé un mouvement du cerveau et du LCR qui semblait lié à l’activité cardiaque et respiratoire.
La masse cérébrale et la moelle se déplaçaient caudalement et médialement (2-3 mm) pendant la systole ; l’inverse se produisait pendant la diastole [11][14].
Lors d’une inspiration, le système nerveux est poussé vers le crâne et le cerveau se rétracte, tandis que lors d’une expiration, le mouvement prédominant est caudal et le cerveau s’expanse [31].
Ces observations montrent que les mouvements du névraxe sont principalement gouvernés par la dynamique cardio-respiratoire, à une fréquence proche de celle de la respiration [32], donc plus rapide que celle habituellement attribuée au MRP/CRI.
Dans l’ensemble, ces données suggèrent que le MRP/CRI n’est pas directement lié à une motilité intrinsèque du cerveau ni au rythme respiratoire.
III.2. Fluctuation du liquide céphalo-rachidien (LCR)
Le LCR est un liquide biologique transparent entourant le cerveau et la moelle épinière, entre la pie-mère et l’arachnoïde, dans l’espace sous-arachnoïdien.
Il a un rôle de protection, et transporte les nutriments et les déchets.
Le LCR est principalement sécrété par filtration du sang au niveau du plexus choroïde des ventricules cérébraux [33].
En tant que liquide, le LCR est peu compressible.
Ainsi, il pourrait pousser les membranes qui feraient bouger les os du crâne.
La théorie initiale était que la circulation pulsatile rythmique du LCR pourrait être à l’origine de l’IRC/MRP.
Le flux du LCR est principalement entraîné par le cycle cardiaque et est donc pulsatile.
Les mouvements du LCR sont également influencés par les mouvements respiratoires, la posture, la pression des veines jugulaires, la pression artérielle et l’activité physique [34][35][30].
Les mouvements de la paroi artérielle constituent le principal moteur du déplacement du LCR, par un mécanisme appelé « pompage périvasculaire » (perivascular pumping). Ainsi, la vitesse du LCR suit étroitement celle des mouvements artériels.
Le volume total est d’environ 150 ml, renouvelé quotidiennement trois à quatre fois (environ 500 ml produits par jour) [36].
La vision dominante est que le LCR descend dans les différents ventricules, puis dans l’espace sous-arachnoïdien pour être finalement réabsorbé principalement au niveau crânien par les systèmes lymphatique et veineux.
Nous savons maintenant que le système veineux ne draine que 30 % du volume total tandis que le système lymphatique nasal constitue en réalité une part majeure du drainage crânien du LCR (40 % du volume total) le long des nerfs crâniens (lame criblée de l’os ethmoïde) [37].
Environ 25 % est drainé au niveau spinal, par les villosités arachnoïdiennes des veines spinales à l’émergence des nerfs spinaux.
Une petite quantité diffuse également légèrement à travers l’arachnoïde et la dure-mère vers les tissus conjonctifs environnants puis vers les réseaux veineux et lymphatiques [37][38].
La théorie de Sutherland postulait que le LCR était en continuité avec le reste de l’organisme, s’étendant vers le système lymphatique, les voies périvasculaires et périneurales.
Cette hypothèse suggère que la perception du rythme du LCR pourrait être ressentie n’importe où sur le corps [2].
Cependant, selon Sakka et al. [38], il n’existe pas de continuité entre le LCR et la périphérie car l’espace sous-arachnoïdien se rétrécit près du pôle proximal du ganglion et se termine dans un cul-de-sac clairement défini anatomiquement.
La continuité se fait avec les espaces périvasculaires ou de Virchow-Robin, qui semblent plutôt drainer le liquide interstitiel du cerveau.
Cependant, les avancées techniques et méthodologiques ont maintenant démontré que le LCR diffuse dans le système nerveux périphérique (SNP).
Une étude de Ligocki et al. a montré que le LCR suit la distribution de nanoparticules d’or de 1,9 nanomètre du SNC vers le SNP au niveau des zones d’attache/transition des racines et se distribue dans le périnèvre et l’endonèvre, atteignant finalement l’axoplasme des nerfs périphériques distaux [39].
Pessa et al. [40] ont montré que la perfusion ventriculaire et les nanoparticules peuvent être utilisées pour identifier le flux du LCR et la circulation glymphatique dans les gaines nerveuses humaines.
Le flux du LCR dans les nerfs peut être conceptualisé comme un système circulatoire ouvert [40].
Au sein du crâne et du canal spinal, la circulation du LCR est soumise aux variations de pression intrathoracique induites par la ventilation.
Lors de la ventilation, le flux du LCR sert à contrebalancer le flux sanguin veineux.
L’inspiration, qu’elle soit volontaire ou forcée, entraîne une augmentation du volume de LCR se dirigeant vers la tête, l’expiration entraînant ensuite un déplacement caudal du flux [41][32].
Ces observations témoignent d’un couplage étroit entre le LCR et le système veineux, qui réagit aux variations de pression induites par la respiration [41][32].
Les trabéculations et les ligaments de l’arachnoïde ralentissent et entravent le flux du LCR, rendant le mouvement plutôt anarchique, et la circulation très lente (1 cm/heure) et ni constante ni linéaire. La vitesse varie selon la localisation : elle est la plus lente aux points les plus éloignés du site de production et des artères crâniennes, avec un flux minimal ou nul observé au niveau lombaire [36].
Il ne semble pas exister de flux et reflux véritablement continu et palpable, pas de rythme dans la production ou le drainage du LCR, qui collerait avec le ressenti des ostéopathes.
En conclusion, un mouvement d’expansion/rétraction du cerveau est lié à la respiration [30] plutôt qu’à des variations de pression du LCR qui sont en réalité trop faibles pour influencer le système crânien [10].
De plus, il n’existe aucune continuité liquidienne entre le réservoir de LCR et la périphérie du corps à aucun point.
Il semble donc difficile d’attribuer les mouvements du LCR à l’IRC/MRP perçu par les ostéopathes.
Le LCR est d’une importance significative dans la philosophie de l’ostéopathie crânienne et, en augmentant les fluctuations, pourrait jouer un rôle crucial dans l’amélioration de l’état d’un patient.
Cependant, il ne semble pas être à l’origine du MRP discuté ici.
III.3. Motilité des membranes intracrâniennes et intraspinales
Les membranes durales font partie des enveloppes membraneuses appelées méninges qui entourent le cerveau et le SNC.
La dure-mère s’attache à certains os crâniens en intracrânien et peut avoir des portions externes à travers les sutures du crâne [42].
En outre, la dure-mère s’attache aux os cervicaux supérieurs et au sacrum, et il existe des attaches tout le long de la colonne vertébrale [43][44][45].
Dans le crâne, la faux du cerveau et la tente du cervelet font partie du système de la dure-mère et forment une structure qui maintient tous les os ensemble.
Sutherland appelait cela la « membrane de tension réciproque » du crâne humain.
Sutherland pensait que les variations de tension de la dure-mère joueraient un rôle dans le déplacement des os auxquels elle est attachée et qu’il ne pourrait y avoir de mécanisme réciproque si elle n’était pas continuellement tendue [3].
Le crâne se déplacerait en rythme, à travers des phases dites d’inspiration et d’expiration, entraîné par le mouvement des tensions changeantes dans les membranes de tension réciproque.
La dure-mère a une épaisseur moyenne d’un millimètre, avec des propriétés viscoélastiques anisotropes (elle n’est donc pas inextensible comme certaines théories ostéopathiques le prétendent) [46].
Les résultats de Al-Habib et al. [47] sont cohérents avec les connaissances anatomiques fondamentales selon lesquelles la dure-mère possède le plus grand degré d’élasticité, suivie par la pie-mère et enfin la moelle épinière [47].
Ils démontrent également que la moelle épinière comprimée présentait une rigidité significativement plus grande par comparaison avec son équivalent non comprimé [47].
Ces résultats sont cohérents avec les résultats de Royo-Salvador et al. [48][49] sur le conflit de croissance craniocervical, où il a été démontré que l’étirement du filum terminale peut entraîner une compression de la moelle épinière, ainsi qu’une traction, tirant ainsi le cervelet dans le foramen magnum.
Les procédures de détachement du filum terminale ont été associées à un déplacement crânial du cône médullaire [48][49].
Les méninges transmettent les forces mécaniques de l’extérieur vers l’intérieur (traumatisme), et de l’intérieur vers l’extérieur [3].
De plus, ce sont des structures qui reflètent les variables mécano-métaboliques de l’environnement dans lequel elles résident, changeant leur capacité à gérer le stress et modifiant leur structure intrinsèque au fil du temps [50].
Selon Bordoni et al., les méninges seraient donc capables de s’adapter aux stress et aux contraintes, et ne sembleraient pas assez rigides pour tirer les os, sauf lorsqu’elles ont tendance à s’ossifier (ce qui peut arriver avec l’âge, en particulier dans les sinus de la dure-mère), affectant la transmission des forces mécaniques [50].
Cependant, au vu des données actuelles, on pourrait supposer que si une tension (pression ou traction) vient du cerveau vers la peau, les différentes couches devraient amortir et ralentir la vitesse de propagation des forces de tension produites [51]. Par conséquent, l’onde de l’IRC/MRP devrait également diminuer avec la distance à l’axe vertébral.
Cependant, les ostéopathes utilisant le MRP/IRC observent et décrivent habituellement une fréquence égale, voire synchrone, en tous les points du corps ; ainsi, cette hypothèse paraît peu probable.
III.4. Mobilité articulaire des os crâniens
La première hypothèse proposée en 1939 par Sutherland était que le MRP ressenti au niveau crânien était dû au mouvement des os crâniens tirés par les membranes, elles-mêmes poussées par la fluctuation du liquide céphalo-rachidien.
Il pensait que le crâne pouvait conserver une flexibilité relative au niveau des sutures du crâne chez l’adulte.
Historiquement, le mouvement des os crâniens était considéré comme une impossibilité anatomique et il reste encore le phénomène le plus controversé du MRP [52].
L’argument principal des défenseurs de la théorie de la mobilité des os du crâne est que les sutures qui articulent les différentes parties du crâne ne s’ossifient jamais complètement [53][54].
Bien que la fermeture des sutures soit un processus graduel, des spicules osseux apparaissent bien avant la fusion complète des sutures [54].
La rigidité du crâne humain augmente avec l’âge avec une énorme variabilité entre les individus et entre les sutures [55].
La calcification de la plupart des sutures commence à l’âge de 20 ou 30 ans [56] et la fin de ce processus est extrêmement variable selon les individus et les types de sutures [57][58][59].
Au-delà de l’âge de 60 ans, la plupart des sutures sont complètement ossifiées [60].
En revanche, les ostéopathes ne rapportent pas de difficulté particulière à percevoir ou à raviver l’IRC/MRP chez les personnes âgées [61].
L’amplitude et la force du MRP ne semblent pas diminuer progressivement avec l’âge, comme on pourrait s’y attendre si elles étaient effectivement liées à une diminution de la mobilité articulaire au sein des sutures à mesure qu’elles fusionnent progressivement au fil du temps.
Dans le modèle crânien ostéopathique, l’articulation qui représente le moteur de la biomécanique crânienne et à laquelle sont attribuées les différentes dysfonctions imaginées par Sutherland est la synchondrose entre l’os occipital et l’os sphénoïde, la fameuse symphyse sphénobasilaire [2][3]. Son processus d’ossification se termine au cours de la puberté [46].
Les sutures du chondrocrâne humain fusionnent progressivement durant l’enfance et l’adolescence, atteignant une fusion complète une fois que la tête a terminé sa croissance [60][62][63].
Ainsi, le crâne adulte possède une symphyse sphénobasilaire ossifiée et, d’un point de vue scientifique, il n’est pas possible de considérer cette articulation comme le principe du mouvement crânien ou comme la cause des diverses dysfonctions décrites en ostéopathie, et les explications des approches manuelles visant à libérer cette articulation ossifiée devraient être reconsidérées [46].
Certains auteurs ont tenté de prouver qu’une pression commune appliquée par le praticien (5 à 10 g) pourrait déplacer les sutures.
Downey et al. [64] ont émis l’hypothèse que de faibles charges appliquées à l’os frontal de lapins anesthésiés, simulant la technique ostéopathique de frontal lift, entraîneraient des changements significatifs et un mouvement au niveau de la suture coronale, mais ils n’ont pas réussi à le prouver.
Une force de 50 kg devrait être appliquée au crâne du lapin pour déplacer une suture de 1 mm, pour un niveau d’ossification comparable à celui d’un humain âgé de 20 à 30 ans [65], et 15 kg pour un enfant humain, ce qui est bien supérieur aux 5 à 10 g recommandés en ostéopathie crânienne [66].
Les scientifiques ont longtemps supposé que les os crâniens étaient fusionnés et ne pouvaient pas bouger, mais il existe maintenant des preuves considérables qu’il existe une flexibilité crânienne [67][55] comme dans le reste des tissus du corps.
Le tissu osseux possède des propriétés viscoélastiques car il contient de l’élastine et du collagène et ensemble ils assurent une capacité de déformation mécanique d’environ 10 %-15 % [46].
Starkey [61] décrit l’anatomie du clivus sphénoïdal et montre qu’il est spongieux et donc malléable, dur et épais et donc immobile.
Cook [68] évoque une flexibilité plutôt qu’une mobilité des os du crâne tandis que Seimetz et al. [55] suggèrent une possible motilité des os crâniens.
Même s’il fait partie des matériaux les plus durs du corps, l’os se déforme pendant la fonction normale et plus évidemment pendant un traumatisme.
Dans de nombreuses études, le mouvement crânien a été induit par diverses contraintes internes et externes sur le crâne à travers des spécimens animaux et humains.
En utilisant l’IRM, Crow et al. [69] ont effectivement observé la variation des mesures de différents points du crâne sans intervention/intention humaine.
Ils ont trouvé des valeurs statistiquement différentes pour la surface, la largeur, la hauteur et les mesures du grand axe, mais pas pour le périmètre et le petit axe, ce qui ne correspond pas à l’expansion et à la rétraction ressenties par les ostéopathes.
Le modèle crânien de Sutherland fait peu référence à l’action des muscles.
Cela est possiblement dû au fait qu’il analysait des os secs, comme cela se faisait dans d’autres premiers modèles ostéopathiques.
Cependant, selon Gabutti et al. [70], une grande quantité de recherches sur les propriétés mécaniques des os crâniens et des sutures confirme que la contraction musculaire est l’une des causes principales de la déflexion des os crâniens [71].
Les sutures crâniennes, en raison de leurs propriétés viscoélastiques et de la constitution de la matrice extracellulaire qui les entoure, riche en fibres de collagène, protéoglycanes et eau, sont évidemment plus flexibles que l’os adjacent [70].
Plutôt qu’une mobilité, les sutures jouent un rôle dans l’absorption de l’énergie et la transmission des forces [72][73].
Les propriétés biomécaniques du crâne humain/de la suture crânienne diffèrent selon l’âge et les couches (diploé, tables interne et externe) [74].
Les sutures peuvent affecter la manière dont la tête se déforme, mais la tête se déforme quand même même si elles sont fusionnées et la densité des sutures (en fonction de leur fermeture) pourrait être un facteur limitant de l’amplitude du mouvement [70].
Pour conclure, il existe bien un mouvement des os du crâne, mais pas nécessairement entre eux.
Les mesures de l’amplitude du mouvement au niveau de la suture sagittale dans les études de Adams et Heisey sont de l’ordre de 300 μm [75][52].
La mobilité crânienne serait donc due à une déformabilité du crâne dans son ensemble, sous l’influence de la pression intracrânienne, de la fluctuation du LCR ou des tensions des membranes et des forces externes telles que les muscles de la tête et leurs tissus conjonctifs, traversés par les vaisseaux sanguins dont la motilité pourrait déformer le crâne [76].
En effet, Moskalenko et al. [76] ont mesuré des changements rythmiques de la forme et du volume du crâne en utilisant des scans NMR sériés.
Ils ont confirmé un taux de 6 à 15 cpm et l’extensibilité physique du crâne osseux et ont observé une expansion du crâne de 0,2 à 0,4 mm immédiatement après l’injection de 20 ml de liquide dans l’artère carotide, et ont ainsi vérifié l’effectivité de l’augmentation du volume crânien [76].
La mobilité crânienne serait donc davantage une conséquence qu’une composante du MRP, un effet plutôt qu’une cause, et nous devons reconsidérer le modèle de Sutherland.
Du point de vue du traitement ostéopathique, nous ne remettons pas en question la possibilité de libérer, comme n’importe quel autre fascia, une suture crânienne de sa tension, quel que soit son niveau d’ossification.
On pourrait imaginer, comme dans l’article de Hamm [77], qu’une densification des tissus par polymérisation des fibres de collagène solidifie les deux bords d’une suture et provoque une fixation [77].
Le traitement ostéopathique crânien consisterait alors à assouplir la zone comme à d’autres niveaux du corps mais pas nécessairement à restaurer un mouvement des os du crâne entre eux.
III.5. Le mouvement involontaire du sacrum entre les os iliaques. L’hypothèse du « core link »
Sutherland suggérait que la dure-mère était inextensible, de sorte que la traction venant du crâne en relation avec le mouvement des os crâniens entraînerait le mouvement du sacrum [2][3].
Cependant, si la dure-mère était si rigide, pourrions-nous nous pencher ?
En réalité, elle possède une élasticité et des expériences montrent que dans une position neutre de la colonne vertébrale, la gaine dure-spinale présente des plis, suggérant que les tissus sont relâchés [78].
L’étude de Al-Habib et al. [47] démontre que la dure-mère présente un degré d’élasticité double de celui de la pie-mère, et triple de celui de la moelle épinière [47].
On observe que la longueur du canal spinal varie entre la flexion et l’extension de la colonne de 19,4 mm ± 6,4 mm [79].
Par conséquent, il n’existe aucune étude concrète pour prouver cette théorie.
Cella et al. [80] ont étudié la connexion occiput-sacrum d’un point de vue neurophysiologique.
La technique sacrée n’a pas produit de changements immédiats sur la puissance alpha de bande du cerveau occipital.
Inversement, la technique crânienne « compression du quatrième ventricule » (CV4), comme des preuves antérieures le soutenaient [81], a généré des effets immédiats, suggérant une base biologique différente pour la connexion entre la tête et le sacrum dans la thérapie ostéopathique.
De ce pilier émerge l’idée d’une unité et d’une synchronisation des fréquences observées au niveau du crâne et du bassin, et par extension dans tout le corps.
Tous les ostéopathes ne sont pas d’accord sur ce point.
Moran et Gibbons [82] n’ont pas pu démontrer une synchronisation entre les rythmes palpés de la tête et du sacrum.
Rogers et al. [83] n’ont montré aucune correspondance entre les rythmes de la tête et du pied lorsque deux examinateurs palpèrent simultanément le MRP.
On peut émettre l’hypothèse que les résultats auraient pu être différents s’ils avaient d’abord « rééquilibré » leurs patients.
Il serait intéressant de mener d’autres études expérimentales mesurant le MRP à différents sites corporels, avant et après des séances d’ostéopathie, avec les mêmes praticiens et avec des praticiens différents, de manière aveugle.
Au vu des résultats de Al-Habib et al. [47] et de Royo-Salvador et al. [48][49], dans le cas d’une transmission d’un mouvement se propageant du crâne au sacrum, celle-ci devrait être transmise par la moelle et le filum terminale, qui est attaché au coccyx et non au sacrum [47][48][49].
Cela ne correspond pas au modèle de Sutherland [2][3].
En conclusion de cette partie, nous avons montré que la conception de 1939 de Sutherland de la base physiologique de l’IRC/MRP, encore enseignée comme un dogme, est remise en question par les connaissances scientifiques actuelles.
Nous allons maintenant passer en revue diverses hypothèses ou nouveaux modèles explicatifs qui pourraient être pris en considération et confrontés aux données scientifiques afin de voir émerger un futur modèle consensuel.
IV. IRC/MRP et vasomotion
Le MRP est un mécanisme qui produit un mouvement cyclique, perceptible sous les mains partout sur le corps, et pas seulement autour du crâne (IRC).
Jones [84] a d’abord démontré en 1850 une rythmicité vasculaire sur la surface ventrale de l’aile d’une chauve-souris, indépendante des rythmes systolique et respiratoire, correspondant à une variation rythmique spontanée du diamètre des veines, induite par des contractions intermittentes des muscles lisses des parois des micro-vaisseaux, provoquant un déplacement actif du sang sous la forme d’une oscillation lente.
Il a appelé cette oscillation flowmotion, mais nous utilisons maintenant le terme de vasomotion ou vasomotricité.
La vasomotion correspond à la capacité des vaisseaux sanguins ou lymphatiques à se contracter ou se dilater, afin de moduler le flux, en réponse à des variations de pression [85].
Au niveau artériel, les gros vaisseaux (aorte, artères de gros calibre) présentent essentiellement des réponses passives en raison de l’abondance de fibres élastiques dans leurs tuniques (appelée compliance ou distensibilité artérielle), qui servent à atténuer les conséquences de la systole ventriculaire sur la pression artérielle (PA) [86].
En diastole, les gros troncs retrouvent leur diamètre comme un ballon qui se dégonfle, ce qui limite la diminution de la pression artérielle [86].
Deux autres mécanismes, liés à la présence de cellules musculaires lisses vasculaires (VSMC), sont présents uniquement dans les petites artères de résistance et les artérioles dont la média (couche médiale) est riche en VSMC, contrairement aux capillaires et aux gros troncs artériels qui en sont dépourvus.
Le premier mécanisme est myogénique et le second neurogénique, souvent source de confusion dans la littérature lorsque les auteurs ne précisent pas auquel des deux ils se réfèrent.
La vasomotion est d’une importance particulière dans l’étude des troubles vasculaires, comme en témoignent les résultats de Fredriksson et al. [87].
Leurs recherches, qui ont utilisé la spectroscopie proche infrarouge (NIRS) pour mesurer de faibles et très faibles oscillations hémodynamiques spontanées (0,003-0,15 Hz), ont corroboré les résultats de Stefanovska et al. [88].
Cette dernière étude a montré une distribution des fréquences de vasomotion comme suit : endothéliale (0,0095-0,02 Hz), neurogénique (0,02-0,06 Hz), myogénique (0,06-0,15 Hz), respiratoire (0,15-0,4 Hz) et cardiaque (0,4-1,6 Hz) [88].
Parlons d’abord du mécanisme myogénique, qui semble être le plus pris en compte dans l’étude de la vasomotion.
Les artères de petit diamètre se contractent en réponse à une augmentation aiguë de la pression artérielle et inversement se relâchent lorsque la pression artérielle baisse [89][90].
Aux bifurcations artériolaires, les cellules montrent une activité de pacemaker générée par l’oscillation spontanée de la concentration intracellulaire en ion Ca2+ dans les muscles lisses situés dans les parois mêmes des vaisseaux [91][90][92].
Ces cellules répondent également à divers signaux, d’origine adrénergique (vasoconstricteurs), cholinergique (vasodilatateurs), métabolique (pH, CO2, ATP, NO et O2), humorale (prostaglandines, EDRF, etc.) et myogénique (température et pression musculaire locale) [90].
Dans l’article de Colantuoni et al. [93] sur l’étude de la vasomotion artériolaire et de la régulation du flux sanguin, la principale caractéristique de la microvascularisation artériolaire a été identifiée comme étant les variations de diamètre en fonction du temps, dont les fréquences fondamentales ont été déterminées par analyse spectrale.
On a trouvé que la fréquence fondamentale variait approximativement de 4 à 15 cpm dans les artérioles de rang 1 (8 micromètres) et de 2 à 11 cpm dans les artérioles de rang 2 (10 à 13 micromètres).
Les vaisseaux d’ordres 3 et 4 (20 et 30 micromètres, respectivement) présentaient une fréquence fondamentale allant de 0,5 à 6 cpm et de 0,3 à 3 cpm, respectivement [93].
Les oscillations sont synchronisées par des phénomènes électriques liés à l’oscillation du potentiel de membrane cellulaire (polarisation-dépolarisation), qui est transmise à toutes les cellules couplées par des jonctions gap, même celles sans fonction pacemaker [94][95].
La conduction longitudinale des réponses vasomotrices est un processus vital qui permet l’orchestration des altérations de diamètre et de la distribution du flux entre les vaisseaux.
Elle participe à l’ajustement de la résistance vasculaire en assurant une coordination entre les segments proximaux et distaux au sein de la microcirculation [96].
Les influences neurogéniques ne lui sont pas essentielles, mais la stimulation adrénergique les renforce.
Cette variation n’est donc ni rythmique ni cyclique ni synchrone avec les vaisseaux voisins.
Il s’agit plutôt d’un phénomène localisé et intermittent, ce qui le rend difficile à associer directement au MRP/IRC.
Nilsson et Aalkjaer [91] ont observé que : « Dans de nombreux contextes expérimentaux, la vasomotion pose problème ; par exemple, il est difficile de définir précisément le niveau de tonus d’un vaisseau oscillant. De plus, la vasomotion est souvent imprévisible et difficile à reproduire ; il arrive que des cobayes cessent de présenter une vasomotion pendant des périodes variables, et que des expériences in vivo échouent parce que la vasomotion ne peut pas être reproduite. ».
Hamm [77] conclut : « La présence ainsi que l’intensité ou l’ampleur de la vasomotion sont hautement variables. »
La vasomotion n’est pas systématiquement présente dans des conditions physiologiques « normales » [97].
Elle est généralement plus fréquente dans des conditions de perfusion réduite et est initiée par un stress métabolique mais est habituellement absente au repos [94].
La vasomotion peut n’être présente que pendant de brèves périodes [77].
En conclusion, la vasomotion due au mécanisme myogénique pourrait influencer l’IRC/MRP mais ne peut pas en être l’unique explication.
Si elle joue effectivement un rôle, ses caractéristiques imprévisibles peuvent expliquer nombre des critiques concernant les tests de fiabilité inter/intra-examinateur.
Cependant, Nilsson & Aalkjaer [91] ont observé des vasoconstrictions rythmiques, probablement d’origine neurogénique, les plus grandes artérioles transversales ayant les fréquences les plus basses, allant de 0,3 à 3 cycles/min avec une amplitude de variation de diamètre comprise entre 5 % et 20 % de leur diamètre moyen [91].
Les artérioles d’environ 18 μm de diamètre ont des amplitudes de variation de 15 % à 50 % du diamètre moyen et des fréquences de 0,5 à 6 cycles/min.
Les artérioles d’environ 11 μm de diamètre ont des amplitudes de variation de 50 % à 100 % du diamètre moyen et des fréquences de 2 à 11 cycles/min, et les plus petites, dites artérioles terminales, les plus superficielles, ont les fréquences les plus rapides (4 à 15 cpm), et la plus grande amplitude puisqu’elles varient de 60 % à 100 % du diamètre moyen.
Fait intéressant, dans leur étude, réalisée chez le hamster, les auteurs Nilsson & Aalkjaer [91] soulignent une prédominance des ondes à 0,1 Hz, transmises au début des artérioles de taille moyenne (type 3 selon la classification de Strahler) et réverbérées dans les plus petites artérioles (type 2 et 1), une fréquence similaire à celle du MRP [91].
Cela suggère qu’il existe une superposition de différents rythmes artériolaires, ceux qui sont les plus faciles à percevoir par la main de l’ostéopathe étant probablement les plus superficiels impulsés par les plus petites artérioles.
Villermain-Lecolier et al. [98][99] ont décrit l’existence de micro-mouvements périodiques perçus au niveau de la peau avec une amplitude d’environ 20 à 50 µm, avec des rythmes différents des rythmes cardiaque et respiratoire, également mesurés sur le sujet.
La fréquence de ces mouvements était de 9,73 ± 3,48 cpm.
Selon eux, le MRP était la manifestation d’une vasomotricité locale, et il n’était pas nécessaire qu’il soit synchrone en un point quelconque du corps.
Comme mentionné précédemment, il n’existe manifestement pas de consensus parmi les ostéopathes sur cette question.
La vasomotricité assure une meilleure circulation sanguine et une meilleure perfusion des tissus et contribue ainsi à une meilleure vitalité de l’organisme.
Explorer un lien entre l’IRC/MRP et la vasomotion s’aligne avec un principe fondamental de l’ostéopathie : l’importance de la circulation dans le maintien de la santé, comme l’a souligné Still [100].
La vasomotion pourrait faire partie du mécanisme sous-jacent à l’IRC/MRP, mais probablement pas en être la seule origine, comme nous le verrons dans le paragraphe suivant.
V. IRC/MRP et système nerveux autonome
V.1. IRC/MRP et ondes THM
Les ondes vasomotrices ou ondes de Traube-Hering Mayer (THM) sont des ondes physiologiques normales qui sont générées par des pulsations spontanées des vaisseaux artériels, veineux et lymphatiques.
Les ondes de Traube-Hering sont formées par l’interaction de l’arythmie sinusale respiratoire et de la modulation de la pression pulsée chez des hommes sains [101].
Les ondes THM sont médiées par le système nerveux autonome et, avec l’augmentation de la variabilité de la fréquence cardiaque, sont considérées comme des marqueurs d’un bon équilibre autonome [36].
Les mécanismes neurogéniques influençant la vasomotion sont présents dans des conditions normales.
Ce mécanisme génère des contractions rythmiques et synchrones activées par le SNS et provoque ces oscillations de la pression artérielle, appelées ondes de Mayer [102].
Ces ondes sont également des réponses baroréflexes aux variations de la pression artérielle [103], et sont donc le résultat d’un phénomène de résonance dans la boucle baroréflexe sympathique [104].
Des signaux afférents provenant des artères conductrices initieraient une boucle de rétroaction baroréflexe, relayée à travers le Nucleus Tractus Solitarius (NTS) et transmise via les nerfs vasoconstricteurs sympathiques (chaîne ganglionnaire) aux artérioles, déclenchant ainsi une vasomotion associée aux ondes de Mayer [91].
Le NTS est situé dans le plancher du IVe ventricule ; fait intéressant, c’est la même localisation que celle de la soi-disant « compression occipitale » ou CV4, une technique bien connue en ostéopathie crânienne pour raviver le MRP.
Dans les circulations régionales, les ondes de Mayer sont transmises aux artères conductrices [102], bien qu’atténuées par la compliance locale, et sont détectables dans certains lits vasculaires périphériques, par exemple dans les doigts, ce qui peut être mesuré par photopléthysmographie (PPG) [105].
Cette bande des ondes de Mayer (0,04-0,15 Hz) correspond à la composante basse fréquence (LF) de la variabilité de la fréquence cardiaque, associée à des stimuli provenant des barorécepteurs et des chémorécepteurs du sinus carotidien circulant à travers le SNS jusqu’aux cellules musculaires lisses vasculaires (VSMCs), à laquelle s’ajoute la composante haute fréquence (HF) ou arythmie sinusale respiratoire, également connue sous le nom de bande d’ondes TH (Traube Hering), synchrone avec les mouvements respiratoires (0,15-0,4 Hz) [106].
Les ondes de Mayer montrent une cohérence forte et significative (force du couplage linéaire entre les fluctuations de deux variables dans le domaine fréquentiel) avec l’activité sympathique efférente [107].
Au sein d’une espèce biologique donnée, leur fréquence est assez stable ; chez l’humain, il a été montré que cette fréquence ne dépend ni du sexe, ni de l’âge, ni de la posture [107], mais, dans une large mesure, du délai de la réponse vasculaire à un changement de l’activité nerveuse sympathique.
Ce délai dépend lui-même de la longueur des neurones sympathiques post-ganglionnaires (fibres myélinisées A de conduction inférieure), et donc, en fin de compte, de la taille de l’animal considéré.
Plus l’animal est grand, plus la longueur des fibres est importante, plus le délai est long, plus la fréquence est basse (par ex. 0,1 Hz chez l’humain, 0,3 Hz chez le lapin et 0,4 Hz chez le rat) [108][102].
C’est aussi une observation faite en ostéopathie animale concernant la fréquence du MRP : plus l’animal est grand, plus la fréquence est basse.
Fernandez & Lecine ont probablement été les premiers à enregistrer l’onde vasomotrice tout en la comparant simultanément à la palpation crânienne [109].
Le groupe de Nelson et al. [17][17] a également montré une bonne corrélation (N 328 paires de données ; corrélation, 1,00 ; sig., 0,00) entre la palpation de l’IRC et l’enregistrement de l’onde THM (rapport 2:1) au moyen d’un laser-Doppler, qui mesure la vitesse du flux sanguin par changement de vitesse des érythrocytes (hémoglobine) dans les capillaires sous-cutanés [110].
Comme d’autres auteurs, ils ont confondu les fréquences des ondes de Traube-Hering, des ondes de Mayer, et des deux mélangées (THM) et il n’était pas évident d’apporter de la clarté sur le sujet.
Ils ont conclu que le MRP/IRC et les oscillations THM étaient simultanés, sinon le même phénomène.
Cela a ouvert de nouvelles explications possibles pour les concepts théoriques de base du MRP/IRC et de la thérapie crânienne.
Ils ont attribué le phénomène d’un « still point » à une brève cessation du rythme du MRP dans 79 % des cas avec une diminution de l’amplitude TH.
Hamm explique que McGrath, en examinant l’article de Ferguson, a proposé une explication similaire [77], suggérant que l’IRC est « une manifestation d’un phénomène de flux sanguin extracrânien ».
Christ et al. [111][111] ont mesuré des changements cycliques du volume des membres dans la gamme de l’IRC et ont suggéré qu’ils étaient dus à des changements de la pression artérielle, à la vasomotion artériolaire, et possiblement au diamètre lymphatique.
Ils ont trouvé une correspondance entre des augmentations cycliques du volume artériel et des changements du volume du membre (<0,177 ml pour 100 ml de tissu).
Les muscles sont essentiellement incompressibles [112] et il n’existe pas d’espaces vides dans les tissus environnants qui pourraient absorber ces changements de volume, ce qui signifie qu’une dilatation et une contraction cycliques de ces tubes fasciaux en sympathie avec les changements du volume vasculaire (à la fois intra- et extra-musculaire) pourraient être capables d’influencer d’une manière particulière les configurations de fibres hélicoïdales croisées au sein de leurs parois [113].
Si cela est effectivement lié, cela pourrait expliquer la sensation hélicoïdale (rotation externe et interne) que les ostéopathes ont lorsqu’ils perçoivent le MRP sur les membres.
Au niveau crânien, Abenavoli et al. [114][115] ont conclu que les ostéopathes pouvaient détecter un changement d’amplitude de l’IRC après application du test Q (test de Queckenstedt, une compression bilatérale des veines jugulaires internes qui produisait une augmentation de la pression intracrânienne), montrant que le flux et la pression des veines et des artères pourraient faire partie de l’origine et de la perception de l’IRC/MRP.
Les ondes de Mayer sont abolies, ou du moins fortement atténuées, par le blocage pharmacologique des alpha-adrénorécepteurs [102], ainsi la base hémodynamique des ondes de Mayer serait des oscillations du tonus vasomoteur sympathique des vaisseaux sanguins artériels.
À l’inverse, le blocage aigu des bêta-adrénorécepteurs a des effets mineurs, voire nuls, sur ces oscillations [108][116], suggérant un faible impact du contrôle vagal.
L’urémie entraînerait également une réduction dramatique de l’amplitude des ondes de Mayer, ce qui pourrait indiquer une altération du fonctionnement du système nerveux autonome cardiovasculaire [117].
Il pourrait être intéressant d’étudier la variation potentielle du MRP chez des patients dans de telles conditions.
En conclusion, les ondes de Traube Hering et de Mayer doivent être différenciées l’une de l’autre, et elles pourraient toutes deux contribuer à l’IRC/MRP
V.2. IRC/MRP et variabilité de la fréquence cardiaque (HRV)
Le cœur ne bat pas avec la régularité d’un métronome : le temps entre deux battements cardiaques consécutifs varie continuellement et est connu sous le nom de variabilité de la fréquence cardiaque (HRV) [118].
La HRV est un indicateur reconnu de la santé du système nerveux autonome d’un individu [119].
En général, une HRV élevée peut être considérée comme un signe d’un système nerveux autonome sain et adaptatif, qui ajuste facilement la fréquence cardiaque en réponse aux changements de l’environnement interne ou externe [120].
À l’inverse, une HRV faible est observée dans une variété de conditions pathologiques, incluant les maladies cardiovasculaires et la neuropathie diabétique, et indique une capacité diminuée du système nerveux autonome à répondre aux changements environnementaux [121].
L’analyse de la HRV est une mesure objective non invasive qui peut être utilisée dans des contextes expérimentaux pour mesurer la modulation du SNA, fournissant ainsi des informations sur les niveaux d’activité sympathique et parasympathique.
Contrairement au concept selon lequel les systèmes sympathique et parasympathique agissent de manière holistique et antagoniste, il est désormais reconnu que les deux systèmes fonctionnent de manière coordonnée, parfois de façon synergique, parfois de manière réciproque [122].
L’analyse spectrale de la HRV est traditionnellement divisée en bandes de basse fréquence (LF ; 0,04–0,15 Hz) et de haute fréquence (HF ; 0,15–0,4 Hz).
Cependant, il existe une variabilité dans les définitions des limites de ces bandes de HRV, qui décrivent la régulation du SNA cardiaque.
La HF-HRV, associée à l’arythmie sinusale respiratoire, augmente avec une activité parasympathique (vagale) accrue [123].
À l’inverse, la LF-HRV reflète à la fois des influences sympathiques et parasympathiques et peut représenter un mécanisme physiologique indépendant en plus de ses contributions parasympathiques dominantes [123].
Certaines études proposent que la bande LF reflète une activité subharmonique d’un pacemaker central situé dans le tronc cérébral inférieur [123].
Le ratio LF/HF (basse fréquence sur haute fréquence) a longtemps été considéré comme un indicateur de l’équilibre sympatho-vagal.
Cependant, cette position a fait l’objet de critiques importantes.
Notamment, puisque la bande LF ne reflète pas de manière fiable l’activité sympathique, il existe désormais un consensus selon lequel les mécanismes physiologiques sous-jacents au ratio LF/HF restent incertains, rendant l’interprétation des données LF/HF hautement problématique [124].
Les mesures couramment rapportées de la HRV médiée par le vague sont la HRV haute fréquence (HF-HRV), la HRV basse fréquence (LF-HRV).
Plus récemment, une bande de fréquence intermédiaire (IM) (une activité émergeant dans divers systèmes périphériques chez l’humain lors d’une relaxation hypnoïde) a été incluse dans les analyses physiologiques systémiques du SNA de la perfusion cutanée du front (SP), de l’ECG, et de la respiration [123][125].
Des données préliminaires suggèrent que ces ondes de 0,15 Hz prennent origine dans le tronc cérébral et se propagent vers la microvascularisation cutanée via les nerfs parasympathiques [123][125].
Schwerdtfeger et al. [126] suggèrent également deux rythmes dans la bande LF, l’un plus bas entre 0,06 et 0,1 Hz et un plus élevé entre 0,1 et 0,14 Hz.
Ils proposent que la bande inférieure reflète principalement la régulation de la pression artérielle par le baroréflexe (fibres nerveuses sympathiques) et que la bande supérieure pourrait fournir des informations sur l’interaction complexe entre les efférences parasympathiques et sympathiques qui signalent les interactions entre le cœur et le cerveau.
Pelz et al. [9] ont montré que le flux sanguin cutané présente des parallèles avec le MRP/IRC en utilisant des mesures de photopléthysmographie (PPG), suggérant que l’IRC/MRP pourrait être une manifestation de cette physiologie de « bande de rythme à 0,15 Hz », également appelée bande intermédiaire (IM).
Par conséquent, la HRV pourrait également contribuer à l’IRC/MRP [127].
VI. MRP, microcirculation, système lymphatique, matrice extracellulaire et réseau fascial
VI.1. Microcirculation
Environ 10 à 20 % du liquide provenant du lit capillaire qui entre dans l’espace interstitiel est renvoyé vers la circulation générale via le système lymphatique, tandis que la majorité (80 à 90 %) réintègre les capillaires et quitte la région via le système veineux [128].
Les veinules ont un diamètre plus large et des parois musculaires plus fines comparées aux artérioles.
Ces veinules sont contrôlées par le système nerveux sympathique, permettant à leurs parois de se contracter et de se relâcher.
Cette action joue un rôle significatif dans la capacitance du système vasculaire, la régulation de la perfusion tissulaire, et sert de mécanisme physique pour la modulation de fréquence observée dans les formes d’onde TH et M [129][130][128].
À mesure que le système vasculaire fluctue avec les oscillations TH et M et, de concert avec la résistance artérielle, le compartiment veineux se contracte lentement et régulièrement.
Cette fluctuation facilite simultanément le mouvement des fluides à travers l’interstitium, la circulation lymphatique, et le retour du sang veineux vers le cœur [131][128].
La vasomotion résultant des oscillations TH et M rend compte de la pression interstitielle négative de l’équilibre de Starling pour les échanges capillaires [128].
Des « ondes d’oxygène disponibles » oscillantes ont également été décrites dans une étude de Vern et al. [132] avec une fréquence moyenne de 9,58 ± 0,117 cpm et dans une étude de Clark et al. [133] avec une fréquence de 6-12 cpm.
Ces données suggèrent que les augmentations cycliques du métabolisme oxydatif cortical représentent le processus oscillatoire local primaire, suivies de modifications hémodynamiques réflexes qui affectent la perfusion tissulaire locale et le volume sanguin intracrânien.
Bien que ce processus ne se produise pas de manière synchrone dans l’ensemble du cerveau, les fréquences relativement proches de l’état redox du cytochrome oxydase et des oscillations THM pourraient également permettre aux deux processus de s’entrainer mutuellement, reliant ainsi le contrôle local et central de la perfusion tissulaire [128][134].
VI.2. Systèmes lymphatique et glymphatique, volume cellulaire cérébral et matrice extracellulaire
La pression du liquide tissulaire est un déterminant du transfert de fluide entre le sang et les espaces tissulaires et entre les espaces tissulaires et les vaisseaux lymphatiques terminaux [135].
Les lymphatiques présentent des contractions rythmiques (muscles lisses des lymphangions) à l’origine d’une onde péristaltique permettant la progression de la lymphe, de fréquence variable : moyenne de 2-2,5 cpm et valeurs allant de 1 à 4 cpm pour Mawhinney et Roddie [136] [136] ; 4 à 5 cpm pour McHale et al. dans les lymphatiques mésentériques bovins [137] ; 4,8 cpm dans les vaisseaux poplités du mouton [138].
Les vaisseaux lymphatiques présentent des contractions spontanées variant de 1 à 30 cpm [139].
Olszewski [140] a rapporté une contractilité vasculaire lymphatique spontanée à un rythme de 1 à 9 (moyenne 4) cpm, indépendante du pouls artériel, de la respiration et des mouvements du corps.
Chaque lymphangion est également capable d’une contractilité spontanée indépendante, par un même mécanisme de réponse myogénique que celui décrit précédemment pour les artères [128].
Bien que les lymphangions puissent se contracter de manière aléatoire via un pacemaker situé dans la paroi du lymphangion juste en amont de la valve, ils fonctionnent plus efficacement lorsqu’ils se contractent de manière synchrone et les vaisseaux lymphatiques tendent à développer facilement une activité synchrone [141][128].
Encore une fois, l’entrainement induit par les ondes THM assure probablement une efficacité optimale de cet aspect du mécanisme.
Les auteurs décrivent des recherches humaines et animales montrant qu’une contraction lymphatique spontanée rythmique se produit chez de nombreuses espèces, y compris chez l’humain.
Par exemple, le canal thoracique chez l’humain se contracte une fois toutes les 10-15 secondes [142], soit environ quatre pulsations par minute, proche du rythme de l’IRC.
Perrin [143] suggère également que le MRP pourrait correspondre à une contraction rythmique des vaisseaux lymphatiques.
Ferguson [10] a affirmé : « As there are not large lymph vessels within the cranium it is unlikely that the lymphatic system causes the CRI ».
Cependant, depuis lors, le groupe de Kipnis a montré qu’il existe des vaisseaux lymphatiques entourant le cerveau [144].
Dans tous les cas, est-il pertinent de rechercher l’origine du MRP dans le crâne ?
En effet, des patients présentant un IRC/MRP faible ou imperceptible au niveau du crâne mais bien exprimé au niveau du sacrum ou ailleurs dans le corps suggéreraient le contraire.
Le système glymphatique est l’étude du processus de circulation, d’accumulation et d’élimination de la glympe, un fluide qui circule dans l’interstitium cérébral.
Le système glymphatique est un processus physiologique complexe impliquant trois phases distinctes.
Premièrement, le liquide céphalo-rachidien (LCR) entre dans les espaces périvasculaires.
Deuxièmement, le LCR est ensuite mélangé avec le liquide interstitiel (ISF).
Enfin, le fluide qui a circulé à travers le tissu cérébral est éliminé [145].
Les cellules cérébrales, à la fois les cellules gliales (oligodendrocytes et astrocytes) et les neurones, ont montré des phénomènes de gonflement/dégonflement rythmique initiés par des variations de la concentration intracellulaire en ions calcium et de l’eau associée [16][7][132].
Cependant, la contraction des oligodendrocytes mesurée par Pomerat et al. [146], à laquelle se réfèrent Retzlaff et Mitchell [147], présentait une fréquence beaucoup plus lente (de 4 à 18 minutes) [147][146].
Les cycles de ces ondes calciques intracellulaires ont été enregistrés à des fréquences allant de 0,5 à 12 cpm en concordance également avec le rythme orchestré par les ondes THM et donc le système nerveux autonome [148], à la fois in vitro et in vivo.
Ces transferts ioniques sont également associés à des altérations de la viscosité et de la charge de la matrice.
En outre, la pression de perfusion capillaire, influencée par les ondes THM, provoque une variation rythmique de la viscosité gel/sol de la matrice extracellulaire, qui est un colloïde aux propriétés viscoélastiques.
En effet, Lee [7] décrit comment la microstructure du fascia est constituée d’un réseau de protéoglycanes (PGs), de glycoprotéines (GPs) et de glycosaminoglycanes (GAGs) formant un tamis à travers lequel tous les métabolites dissous passent du capillaire à la cellule et inversement.
Les PGs sont chargés négativement, lient l’eau et naturellement, en raison de leurs propriétés thermodynamiques instables, forment un gel.
L’ensemble de la structure permet à la matrice extracellulaire d’agir comme un semi-conducteur essentiellement instable, un cristal liquide, qui, selon Hamm [77], pourrait constituer une hypothèse pour expliquer l’expérience palpatoire et les revendications thérapeutiques dans la pratique de l’ostéopathie dans le champ crânien à travers un changement cyclique de texture de la MEC, qui pourrait être altérée et densifiée par des tensions fasciales localisées.
En résumé, le flux sanguin est également modulé par la compliance et la résistance vasculaires mais aussi, en fin de compte, par celles des tissus environnants, à savoir la densité locale de la MEC.
La MEC peut se scléroser sous l’effet des contraintes des tensions fasciales, ce qui conduit à une densification et à une polymérisation des fibres de collagène et à des agrégats volumineux d’acide hyaluronique [149].
Ces processus peuvent également faire partie du mécanisme sous-jacent du MRP.
VII. MRP et entrainement
Bien que Ferguson [10] et Perrin [143] aient indiqué que les veines cérébrales n’ont ni valves ni muscles dans leurs parois fines, et donc pas de vasomotion, le rythme perçu par les ostéopathes pourrait provenir des vaisseaux superficiels et sous-cutanés plutôt que des vaisseaux profonds et cérébraux.
Dans l’intervalle de ceux décrits par les ostéopathes, il existe une grande variété de rythmes différents, et il est possible que certains ostéopathes puissent ressentir la résultante de l’ensemble des rythmes tandis que d’autres n’en perçoivent qu’une partie.
Tous ces rythmes sont probablement superposés et s’influencent vraisemblablement les uns les autres, et ce que l’ostéopathe perçoit du bout des doigts est probablement la résultante de toutes ces oscillations.
C’est la théorie développée par McPartland et Mein [150], suggérant que le MRP est un rythme produit par la synchronisation, ou entrainement, de multiples oscillations biologiques à la fois du patient et du praticien.
Cette idée a également été explorée par Norton [151] avec son modèle de pression tissulaire, qui a proposé que l’IRC est associé à des mécanorécepteurs cutanés à adaptation lente à la fois du patient et du praticien, et que les sources des changements de ces pressions tissulaires sont les rythmes respiratoires et cardiovasculaires combinés de l’examinateur et du sujet.
Cela pourrait expliquer pourquoi différents examinateurs ne sont souvent pas d’accord dans leur détermination de la fréquence de l’IRC chez un même sujet, les fréquences cardiaques et respiratoires de repos des examinateurs pouvant être assez différentes [151].
Tiller et al. [152][152] décrivent un événement significatif apparaissant dans les oscillateurs biologiques lorsque les systèmes sympathique et parasympathique deviennent équilibrés.
Les multiples rythmes du corps, incluant la HRV, les ondes THM, la fréquence respiratoire, le temps de transit du pouls et même les ondes cérébrales, se coordonnent alors en harmoniques entre eux.
Ensemble, ils forment une fréquence primaire fondamentale, que les auteurs ont appelée la fréquence d’entrainement [150].
La fréquence d’entrainement mesurée chez des sujets humains sains avec un équilibre sympathique et parasympathique est d’environ 0,1 Hz (6 cpm), et pourrait correspondre au MRP [152].
Si un équilibre est présent au sein du système nerveux autonome, alors les nombreux rythmes du corps s’harmonisent en une fréquence d’entrainement fluctuante, sinusoïdale, forte et coordonnée, qui peut être palpée comme un IRC/MRP fort et sain.
Dans un état sain, on s’attendrait à une synchronie de tous les tissus, dans le sens où tous sont entrainés à un rythme commun inné.
Ainsi, la vitalité, telle qu’évaluée par l’évaluation de l’IRC, dépendrait de l’équilibre sympatho-vagal [153].
Un dysfonctionnement du système nerveux autonome peut modifier la fréquence d’entrainement, entraînant des perturbations du MRP/IRC, altérant sa fréquence, sa force et son amplitude [150].
En présence d’un dysfonctionnement sévère, les rythmes du corps peuvent ne pas se synchroniser, entraînant un MRP/IRC indétectable.
Il devrait être possible de déterminer expérimentalement si la fréquence d’entrainement correspond au rythme du MRP.
VIII. MRP et mouvement embryologique
Un autre modèle appelé Biodynamique a été développé par Rollin Becker dans les années 1930, puis par la suite par James Jealous [150].
En étudiant les écrits de l’embryologiste Blechschmidt, il a été impressionné par la conclusion de Blechschmidt selon laquelle la fonction embryonnaire (mouvement des fluides) crée la forme et précède la structure [154][155].
Blechschmidt a observé attentivement les cellules de l’embryon en développement, qui migrent en se différenciant.
Il a utilisé le terme « Biodynamics » pour décrire ces mouvements.
Jealous a émis l’hypothèse que les forces du développement embryologique ne cessent pas de fonctionner à la naissance, mais sont maintenues tout au long de la vie comme des forces de croissance et de développement, et sont également impliquées dans les processus de guérison.
Il a décrit un rythme plus lent que le MRP/IRC, qu’il a simplement appelé le « 2,5 cpm rate », avec une fréquence de 2,5 cpm [150].
Dans leur article, ils utilisent souvent la terminologie de Sutherland, le « Breath of life » ou la « force thérapeutique », sans mentionner de fréquence spécifique ni d’origine, mais en soulignant que cela est différent du MRP/IRC.
C’est pourquoi nous avons choisi de ne pas développer davantage cette approche, qui est hors sujet puisque nous nous concentrons sur l’origine du MRP/IRC et non sur ses harmoniques ou d’autres rythmes en dehors de sa plage de fréquence.
Cependant, il est intéressant de noter que le MRP pourrait ne pas être la fréquence fondamentale finale.
Sutherland faisait allusion à des rythmes plus profonds, plus subtils, plus difficiles à détecter, en plus de l’IRC [3].
Son élève, Rollin Becker [156], a déclaré que l’IRC se compose de différents composants, une « fast tide » (8-12 cpm), et une « slow tide » (0,6 cpm) [156].
On retrouve également dans la littérature biodynamique la « mid-tide » (2-3 cpm), et la « long tide » (6 cycles toutes les 9/10 minutes) qui pourraient être liées ou similaires au « Breath of Life ».
Ainsi, il pourrait exister différents rythmes, ce qui rend la mesure objective et la comparaison complexes, et peut expliquer pourquoi la reproductibilité intra- et inter-examinateur est difficile à obtenir.
IX. Perspective
Dans cette dernière partie, nous discuterons de l’utilisation de cet IRC/MRP dans la pratique ostéopathique.
IX.1. Le MRP comme outil ostéopathique
En résumé, si les oscillations du MRP correspondent à des variations de la texture du réseau fascial, il représente un outil précieux pour les thérapeutes manuels visant à relâcher les tensions myofasciales.
En effet, le MRP peut servir d’outil diagnostique en reflétant le niveau de tension dans la zone, et il peut guider les techniques du praticien vers la libération tissulaire, car sa qualité (force et amplitude) s’améliorerait avec les propriétés viscoélastiques et la déformabilité du tissu.
Pour valider ce concept, pourrait-on comparer des mesures objectives Myoton dans différentes régions d’un sujet avec la palpation subjective du MRP afin d’évaluer leur corrélation ?
Et si nous réalisions des mesures Myoton chaque seconde ?
Observerions-nous une variation cyclique ?
Une fréquence dans la plage du MRP ?
Cette théorie concerne une approche loco-régionale, mais la compréhension des mécanismes et des origines du MRP met en évidence l’importance de traiter le corps comme un tout unifié — un autre principe fondamental de l’ostéopathie.
En libérant d’abord la connexion cerveau-cœur et en améliorant la fonction du système nerveux autonome (SNA), l’ensemble du corps en bénéficie.
La communauté ostéopathique a longtemps théorisé que le traitement manipulatif ostéopathique (OMT) peut restaurer les fonctions du corps perturbées par des déséquilibres musculo-squelettiques, en induisant une activation autonome, conduisant à une vasodilatation, une relaxation des muscles lisses et une amélioration du flux sanguin [157].
Si le MRP est lié à l’activation autonome, l’utiliser comme outil diagnostique, comme le font de nombreux ostéopathes, pourrait effectivement constituer un retour utile pour s’assurer que la technique appliquée vient de produire un changement significatif.
La plupart des études indiquent généralement une réduction de l’activité sympathique, associée à une augmentation de la modulation parasympathique après OMT [124][158], ce qui favorise la relaxation et diminue l’activité nerveuse sympathique.
Cependant, il est important de considérer que toute forme de thérapie manuelle capable d’induire une relaxation, indépendamment de la méthode spécifique utilisée, influencera la régulation du SNA.
De plus, l’anticipation psychologique et l’expérience associée à l’ostéopathie peuvent produire des effets physiologiques, compliquant l’affirmation qu’une technique de thérapie manuelle particulière provoque directement des résultats spécifiques [159].
Par conséquent, il est toujours préférable de comparer avec un groupe placebo, comme l’ont fait Abenavoli et al. [115] : en cherchant à mesurer la réponse physiologique des niveaux de sAA (Serum Amyloid A) après la technique CV4, ils ont montré un effet positif qui n’était pas significativement différent de la procédure simulée [115].
La technique CV4 est utilisée pour augmenter le MRP et est associée à une diminution du tonus sympathique et à une activation parasympathique [81][160][19].
Nelson et al. ont montré que la CV4 amplifiait les ondes THM tandis que la simple palpation crânienne ne les affectait pas, de sorte qu’elle pourrait servir de placebo [161][19].
Avant cela, Sergueef et al. [20] ont également montré que les manipulations crâniennes, consistant en une équilibration du schéma global de mouvement crânien et de la jonction cranio-cervicale, affectent les oscillations THM [20].
Pelz et al. [9] ont montré des réponses significatives du système nerveux autonome au cranial vault hold (CVH), une intervention ostéopathique spécifique, en observant ses effets sur la LF-HRV, la bande IM, et la fréquence instantanée d’amplitude maximale (MFHA) des signaux PPG.
Plus récemment, ils ont observé une augmentation significative du root mean square of successive differences (RMSSD) de la HRV après CV4 [162].
D’autres études récentes ont utilisé le RMSSD [163], la conductance cutanée [164], ou la HF de la HRV [165] pour démontrer les effets de l’OMT sur le SNA.
Enfin, Fornari et al. ont montré qu’une seule séance d’ostéopathie chez des participants sains induisait une récupération plus rapide de la fréquence cardiaque et de l’équilibre sympathovagal après un stress mental aigu en atténuant fortement le retrait parasympathique et la prédominance sympathique [166].
La manipulation crânienne et/ou de la colonne cervicale pourrait conduire à un meilleur équilibre autonome par une réduction de l’activité nerveuse sympathique et une amélioration de la variabilité de la fréquence cardiaque, une mesure de l’activité parasympathique [167][168][169][36].
Collectivement, ces études suggèrent que l’OMT pourrait moduler le SNA en améliorant la fonction parasympathique et en réduisant la dominance sympathique et que le MRP pourrait être un outil diagnostique utile pour s’assurer que la technique appliquée vient de produire un changement significatif du SNA.
Lorsque le corps est équilibré, les caractéristiques du MRP de force, d’amplitude et de rythme devraient théoriquement être dans la norme.
Il est donc perçu comme fort, autour de 6 cpm chez l’humain, et symétrique dans ses amplitudes d’expansion/flexion/rotation externe, et de rétraction/extension/rotation interne (globalement, les tissus oscillent entre ouverture et fermeture du corps).
Une symétrie doit également être recherchée entre les membres, suggérant une synchronie en tous les points du corps.
Si ce n’est pas le cas, le corps est alors considéré comme déséquilibré, et le traitement ostéopathique est pertinent ; si c’est le cas, le patient est alors considéré comme équilibré, et le traitement ostéopathique est terminé.
Cette synchronie pourrait avoir du sens, considérant que tous les tissus, harmonisés au niveau de la tenségrité, oscillent à l’unisson à la fréquence d’entrainement, comme l’affirme le principe de l’unité du corps, si cher aux ostéopathes.
Cependant, cette synchronisation supposée entre différentes parties du corps n’est pas universellement acceptée par les praticiens.
En effet, des études palpatoires n’ont pas réussi à démontrer un lien clair entre les rythmes palpés au niveau de la tête et du sacrum [170][82][83].
Néanmoins, on peut supposer que cette synchronisation serait plus facile à démontrer chez des sujets équilibrés ayant bénéficié d’une séance ostéopathique préalable
IX.2. Idéomotion
Les mouvements idéomoteurs peuvent être décrits comme des micro-mouvements que nous réalisons inconsciemment et involontairement, qui sont des expressions automatiques d’idées dominantes plutôt que le résultat d’efforts volontaires [171].
Appliqué à la médecine manuelle ostéopathique, le mouvement perçu pourrait en réalité être généré par le thérapeute lors de la palpation.
Les perceptions inconscientes du thérapeute (telles que les attentes, le degré d’empathie, etc.) peuvent influencer la prise de décision et laisser ouverte la possibilité pour le thérapeute de tomber dans une prophétie auto-réalisatrice ou des « effets de confirmation des attentes » [172].
Dans leur revue de la littérature, Shin et al. [173][173] explorent plusieurs perspectives historiques sur le concept d’idéomotion, qui pourraient offrir des éclairages précieux pour comprendre la perception du MRP.
Bien que ces travaux anciens puissent manquer de la rigueur attendue selon les standards scientifiques contemporains, ils mettent en évidence des idées fondamentales : selon Carpenter en 1874, le simple fait d’attendre un résultat suffirait à produire même des mouvements involontaires.
De même, selon Herbart en 1825, les actions peuvent être initiées par l’anticipation ou le désir de produire des effets sensoriels.
Enfin, James en 1890 a soutenu qu’imaginer un mouvement active la réponse motrice correspondante, soulignant l’interaction entre intention mentale et action physique [173].
En extrapolant à la pratique de l’ostéopathie et à la perception du MRP, on pourrait imaginer qu’en recherchant ces micro-mouvements dans les tissus du patient, l’ostéopathe les provoque, induisant ainsi sa propre perception en erreur.
Cependant, si tel est le cas, cela peut ne pas constituer un problème majeur, puisque les tissus ne peuvent répondre qu’en fonction de leurs propres propriétés mécaniques.
S’ils sont libres de tension, leurs propriétés viscoélastiques leur permettront d’absorber les mouvements idéomoteurs, que l’ostéopathe percevra comme un bon MRP.
Si, au contraire, les tissus sont trop tendus, ils répondront moins facilement à ce stimulus, ce qui pourrait se traduire perceptivement par un MRP moins optimal.
Le test peut donc rester pertinent, tout comme les directions supposées.
Même influencé par les actions idéomotrices du praticien, le tissu ne peut répondre qu’en fonction de sa propre résilience, et l’amplitude ne sera symétrique que si la structure est libre de restrictions.
Les sceptiques qui pensent que le MRP/IRC n’existe pas (mais serait seulement une hallucination palpatoire) ont partiellement tort car il existe effectivement un rythme détectable à la fois par des mains entraînées et par des machines.
Les ostéopathes convaincus que leurs sensations sont entièrement objectives ont également tort.
En effet, la réponse idéomotrice pourrait influencer leur perception, les conduisant à ressentir une superposition incohérente de nombreux rythmes à différentes profondeurs, probablement perturbée par leurs propres rythmes fluctuants.
Les ostéopathes qui pensent que la synchronisation ne doit pas être recherchée ont tort, car lorsqu’elle est atteinte, elle pourrait être un signe que les tissus sont suffisamment relâchés pour répondre à l’action idéomotrice (intention) du praticien.
D’un autre côté, les ostéopathes qui pensent que la synchronisation est physiologique ont partiellement tort car, si le MRP est la somme de nombreux rythmes à différents niveaux, elle ne peut pas être systématique en tout point du corps.
IX.3. Respiration en cohérence cardiaque et MRP
L’Ostéopathie vise à améliorer l’autorégulation du corps, supposément en stabilisant les branches sympathique et parasympathique du système nerveux autonome, le MRP/IRC pouvant servir de témoin de cet effet.
Pelz et al. [174] rapportent des réponses rythmiques de la bande IM lors du Cranial Vault Hold (CVH), une technique courante en OCF, comparables aux dynamiques rapportées pour l’activité IM en réponse à un entraînement de relaxation autogène.
Une augmentation de l’amplitude des oscillations perçues est supposée être liée à une harmonisation des rythmes cœur-cerveau-circulatoires et permettre une circulation fluide dans l’organisme.
L’entrainement physiologique est reconnu comme un mécanisme fondamental sous-jacent à la connexion corps-esprit.
Les interventions basées sur l’entrainement peuvent être utilisées pour promouvoir le bien-être en améliorant les fonctions cognitives, motrices et émotionnelles, offrant des stratégies prometteuses de réhabilitation pour l’amélioration de la santé mentale [175].
Blacklaw-Jones présente un modèle qui identifie l’activité piézoélectrique comme un médiateur potentiel des réponses à l’ostéopathie dans le champ crânien (OCF) et explore le rôle des champs magnétiques générés par l’activité électrique du corps.
Selon cette théorie, ces champs magnétiques oscillent en synchronisation avec les ondes électriques, entraînant des vibrations cohérentes des molécules et, par conséquent, des tissus du corps [176].
Blacklaw-Jones suggère en outre que les praticiens en OCF, lorsqu’ils entrent dans un état méditatif ou contemplatif pendant le traitement, peuvent induire des vibrations cohérentes dans leurs propres tissus.
Par contact physique, le champ électromagnétique harmonisé du praticien serait censé transférer de l’énergie au champ moins cohérent du patient, favorisant des changements thérapeutiques [176].
Cette augmentation de la cohérence serait alors supposée améliorer la fonction cellulaire, soutenant ainsi l’autorégulation et l’homéostasie.
L’amplitude du MRP est supposée augmenter lors d’approches corps-esprit telles que le yoga, la méditation basée sur la pleine conscience, la thérapie respiratoire et autres [177][36].
Un aspect commun de ces pratiques est la survenue d’une respiration en cohérence cardiaque, conduisant à un état de bien-être, de plénitude et de réceptivité [178].
La respiration en cohérence cardiaque consiste à inspirer pendant cinq secondes, puis à expirer pendant la même durée (soit un cycle respiratoire de 10 secondes ou 0,1 Hz), ce qui peut également être obtenu simplement en contrôlant sa respiration [179].
La respiration influence la manière dont le système nerveux autonome régule la fréquence cardiaque : l’inspiration inhibe temporairement l’influence du système parasympathique et augmente la fréquence cardiaque, tandis que l’expiration stimule le système parasympathique et diminue la fréquence cardiaque.
En état de cohérence cardiaque, il existe un équilibre sympathique/parasympathique optimal conduisant à une cohérence entre les rythmes cardiaque et respiratoire, avec une variabilité de la fréquence cardiaque maximale, ce qui permet d’augmenter l’adaptabilité du système nerveux autonome, fournissant un contrôle fin de nombreuses fonctions organiques face aux stimuli ou au stress [180][152].
Puisque l’IRC/MRP est probablement le résultat de la somme de tous les rythmes décrits ci-dessus, on peut émettre l’hypothèse que l’IRC et le MRP, sous-tendus par l’activité du SNA, sont à leur intensité maximale lors de la respiration en cohérence cardiaque, permettant aux ostéopathes de mieux les percevoir et favorisant une circulation optimale de tous les fluides (sang, lymphe, LCR, air) dans le corps.
Cela conduirait à un état de bien-être et d’équilibre.
On peut également supposer que synchroniser la respiration du patient et du praticien avec la perception du MRP pendant la séance pourrait avoir un bénéfice supplémentaire.
Des recherches supplémentaires sont nécessaires pour relier le MRP à d’autres pratiques plus étudiées.
X. Conclusion générale
Notre revue a questionné les mécanismes physiologiques sous-jacents au MRP/IRC.
Nous avons discuté les différentes hypothèses proposées pour expliquer ce rythme.
Depuis la théorie de Sutherland, grâce aux progrès scientifiques, les connaissances concernant les mécanismes physiologiques sous-jacents au MRP ont évolué [3].
Bien que les hypothèses de Sutherland soient encore enseignées, l’hypothèse la plus plausible expliquant le MRP/IRC repose sur des modifications rythmiques de la fluidité de la matrice extracellulaire induites par l’entrelacement de divers rythmes physiologiques, principalement pilotés par l’activité du SNA, favorisant le métabolisme et assurant un transit efficace des nutriments et des déchets à travers l’espace extracellulaire [181].
Une augmentation de l’amplitude de ces oscillations conduirait à une synchronisation des rythmes cœur-cerveau-circulation, permettant une circulation optimale de tous les fluides dans l’organisme.
La Figure 2 illustre une vue d’ensemble des différents mécanismes pouvant sous-tendre le rythme MRP/IRC, présentés dans cette revue.
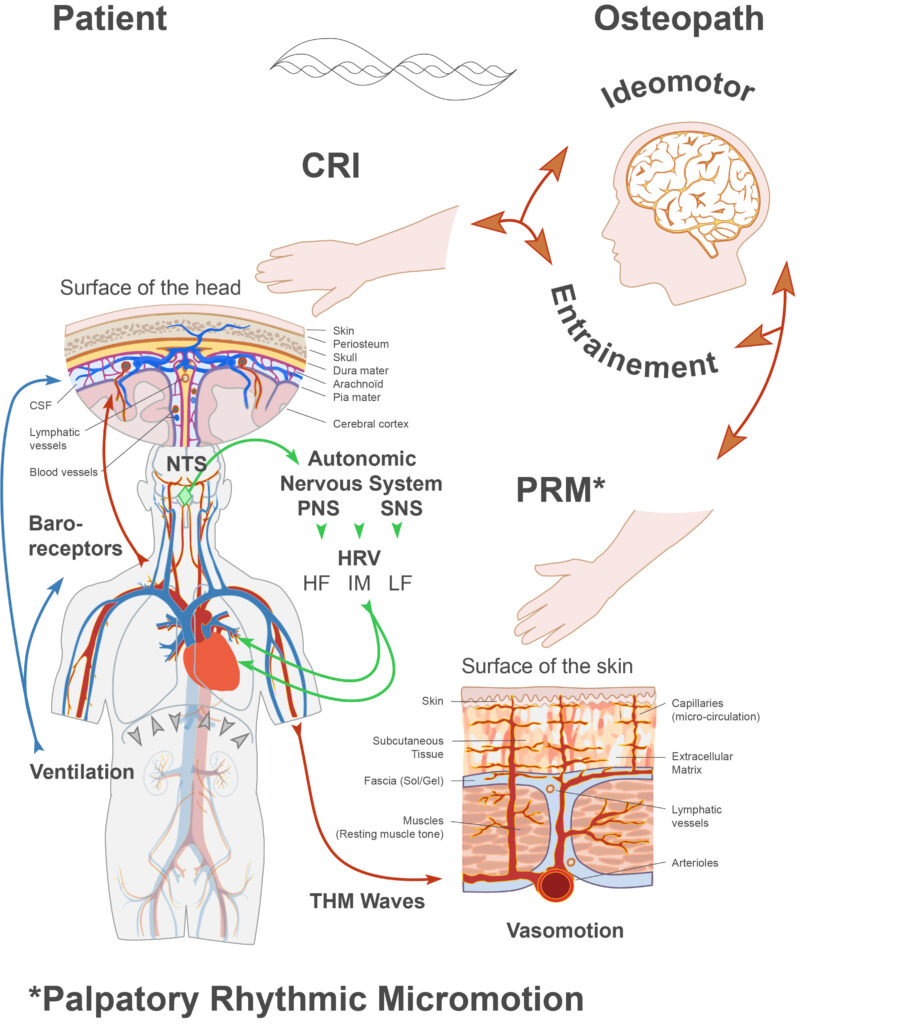
Figure 2. Vue d’ensemble des différents mécanismes sous-jacents au MRP/IRC.
Suite aux changements de paradigme, et afin d’accompagner cette évolution, les auteurs proposent de remplacer le terme dogmatique « Mouvement Respiratoire Primaire » par un terme factuel, « Micromouvement Rythmique Palpatoire » (MRP).
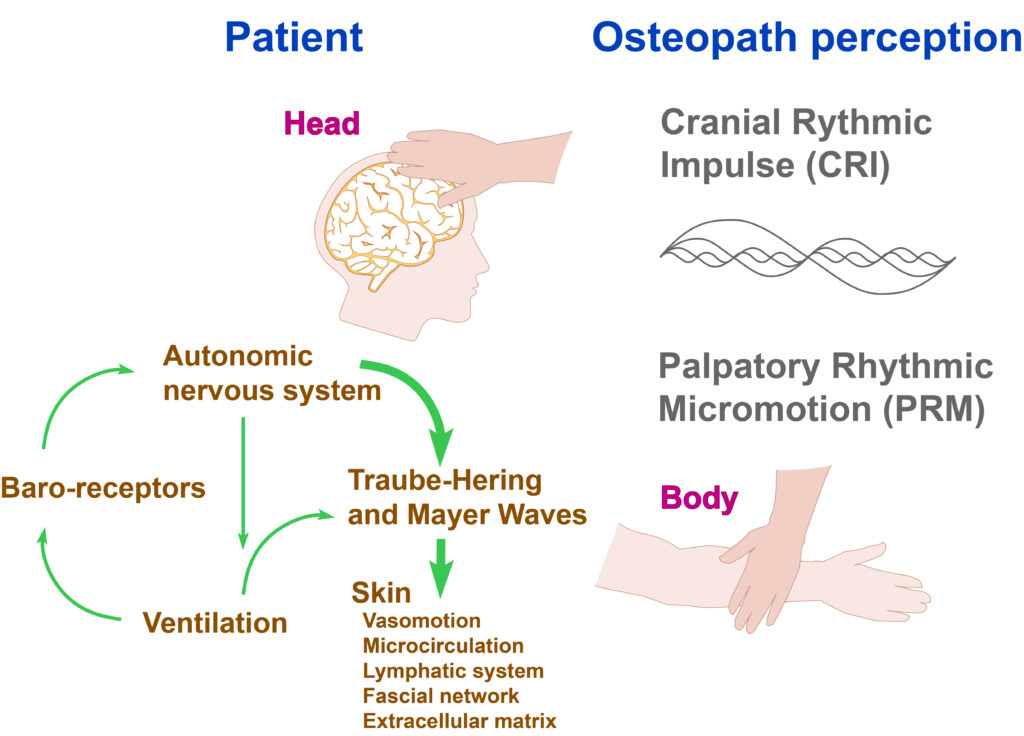
Figure 3. Résumé graphique MRP/IRC
Déclarations
Conflit d’intérêts
Les auteurs déclarent n’avoir aucun intérêt financier ou non financier pertinent à divulguer.
Financement
Aucun financement, subvention ou autre soutien n’a été reçu.
Contribution des auteurs
Tous les auteurs ont contribué à la rédaction de la revue narrative. AG et FM sont à l’origine de l’idée de l’article. LS, AG et FM ont réalisé la recherche bibliographique et l’analyse des données. FM a rédigé la version principale du manuscrit, tandis que LS et AG ont participé à la rédaction et à la révision critique du travail. LS a réalisé une part importante du travail sur les figures. Tous les auteurs ont lu et approuvé la version finale du manuscrit.
Remerciements
Nous remercions chaleureusement Manina Hobson pour sa relecture attentive de l’article en anglais.
Titre court :
Mécanismes physiologiques sous-jacents au PRM/CRI en ostéopathie
Références
- a, b, c, d, e, fMériaux F, Stubbe L, Guyon A (2024). « Physiological Mechanisms Underlying the Primary Respiratory Mechanism (PRM) and Cranial Rhythmic Impulse (CRI) in Osteopathy: A Systematic Review. » Healthcare. 12(24):2503. doi:10.3390/healthcare12242503.
- a, b, c, d, e, f, g, h, i, j, k, lMagoun HI (1976). Osteopathy in the Cranial Field. 3rd ed. Sutherland Cranial Teaching Foundation.
- a, b, c, d, e, f, g, h, i, j, k, lSutherland WG (1990). Teachings in the Science of Osteopathy. SCTF.
- a, b, cRasmussen TR, Meulengracht KC (2021). « Direct measurement of the rhythmic motions of the human head identifies a third rhythm. » Journal of Bodywork and Movement Therapies. 26:24–29. doi:10.1016/j.jbmt.2020.08.018.
- a, bWoods JM, Woods RH (1961). « A physical finding related to psychiatric disorders. » The Journal of the American Osteopathic Association. 60:988–993.
- ^Sergueef N, Greer MA, Nelson KE, Glonek T (2011). « The palpated cranial rhythmic impulse (CRI): Its normative rate and examiner experience. » International Journal of Osteopathic Medicine. 14(1):10–16. doi:10.1016/j.ijosm.2010.11.006.
- a, b, cLee RP (2008). « The Living Matrix: A Model for the Primary Respiratory Mechanism. » EXPLORE: The Journal of Science and Healing. 4(6):374–378. doi:10.1016/j.explore.2008.08.003.
- a, bPelz H, Müller G, Keller M, Mathiak K, Mayer J, Borik S, et al. (2023). « Validation of subjective manual palpation using objective physiological recordings of the cranial rhythmic impulse during osteopathic manipulative intervention. » Scientific Reports. 13(1):Article 1. doi:10.1038/s41598-023-33644-8.
- a, b, c, dPelz H, Müller G, Keller M, Mathiak K, Mayer J, Borik S, et al. (2023a). « Validation of subjective manual palpation using objective physiological recordings of the cranial rhythmic impulse during osteopathic manipulative intervention. » Scientific Reports. 13(1):Article 1. doi:10.1038/s41598-023-33644-8.
- a, b, c, d, e, fFerguson A (2003). « A review of the physiology of cranial osteopathy. » Journal of Osteopathic Medicine. 6(2):74–84. doi:10.1016/S1443-8461(03)80017-5.
- a, bGreitz D (1993). « Cerebrospinal fluid circulation and associated intracranial dynamics. A radiologic investigation using MR imaging and radionuclide cisternography. » Acta Radiologica. Supplementum. 386:1–23.
- a, bJordan T (2009). « Swedenborg’s influence on Sutherland’s ‘Primary Respiratory Mechanism’ model in cranial osteopathy. » International Journal of Osteopathic Medicine. 12(3):100–105. doi:10.1016/j.ijosm.2009.03.006.
- a, bMaier SE, Hardy CJ, Jolesz FA (1994). « Brain and cerebrospinal fluid motion: Real-time quantification with M-mode MR imaging. » Radiology. 193(2):477–483. doi:10.1148/radiology.193.2.7972766.
- a, bPoncelet BP, Wedeen VJ, Weisskoff RM, Cohen MS (1992). « Brain parenchyma motion: Measurement with cine echo-planar MR imaging. » Radiology. 185(3):645–651. doi:10.1148/radiology.185.3.1438740.
- a, bUpledger JE (2004). « CranioSacral Therapy. » Seminars in Integrative Medicine. 2(4):159–166. doi:10.1016/j.sigm.2004.12.002.
- a, bFrymann VM (1971). « A study of the rhythmic motions of the living cranium. » The Journal of the American Osteopathic Association. 70(9):928–945.
- a, b, cNelson KE, Sergueef N, Lipinski CM, Chapman AR, Glonek T (2001). « Cranial rhythmic impulse related to the Traube-Hering-Mayer oscillation: Comparing laser-Doppler flowmetry and palpation. » JAOA: Journal of the American Osteopathic Association. 101(3):163–173.
- ^Nelson KE, Sergueef N, Glonek T (2006a). « Recording the Rate of the Cranial Rhythmic Impulse. » JAOA: Journal of the American Osteopathic Association. 106(6):337–341.
- a, b, cNelson KE, Sergueef N, Glonek T (2006b). « The Effect of an Alternative Medical Procedure Upon Low-Frequency Oscillations in Cutaneous Blood Flow Velocity. » Journal of Manipulative and Physiological Therapeutics. 29(8):626–636. doi:10.1016/j.jmpt.2006.08.007.
- a, b, cSergueef N, Nelson KE, Glonek T (2002). « The effect of cranial manipulation on the Traube-Hering-Mayer oscillation as measured by laser-Doppler flowmetry. » Alternative Therapies in Health and Medicine. 8(6):74–76.
- ^Tricco AC, Lillie E, Zarin W, O’Brien KK, Colquhoun H, Levac D, et al. (2018). « PRISMA Extension for Scoping Reviews (PRISMA-ScR): Checklist and Explanation. » Annals of Internal Medicine. 169(7):467–473. doi:10.7326/M18-0850.
- ^Kellie G (1824). « An Account of the Appearances Observed in the Dissection of Two of Three Individuals Presumed to Have Perished in the Storm of the 3d, and Whose Bodies Were Discovered in the Vicinity of Leith on the Morning of the 4th, November 1821; with Some Reflections on the Pathology of the Brain: Part I. » Transactions. Medico-Chirurgical Society of Edinburgh. 1:84.
- ^Monro A (1783). « Observations on the Structure and Functions of the Nervous System, Illustrated with Tables. » The London Medical Journal. 4(2):113.
- a, bKazimierska A, Manet R, Vallet A, Schmidt E, Czosnyka Z, Czosnyka M, et al. (2023). « Analysis of intracranial pressure pulse waveform in studies on cerebrospinal compliance: A narrative review. » Physiological Measurement. 44(10). doi:10.1088/1361-6579/ad0020.
- ^Brasil S, Solla DJF, Nogueira R de C, Teixeira MJ, Malbouisson LMS, Paiva W da S (2021). « A Novel Noninvasive Technique for Intracranial Pressure Waveform Monitoring in Critical Care. » Journal of Personalized Medicine. 11(12):Article 12. doi:10.3390/jpm11121302.
- ^de Moraes FM, Rocha E, Barros FCD, Freitas FGR, Miranda M, Valiente RA, et al. (2022). « Waveform Morphology as a Surrogate for ICP Monitoring: A Comparison Between an Invasive and a Noninvasive Method. » Neurocritical Care. 37(1):219–227. doi:10.1007/s12028-022-01477-4.
- ^Godoy DA, Brasil S, Iaccarino C, Paiva W, Rubiano AM (2023). « The intracranial compartmental syndrome: A proposed model for acute brain injury monitoring and management. » Critical Care. 27:137. doi:10.1186/s13054-023-04427-4.
- ^Pitlyk PJ, Piantanida TP, Ploeger DW (1985). « Noninvasive intracranial pressure monitoring. » Neurosurgery. 17(4):581–584. doi:10.1227/00006123-198510000-00008.
- ^Kasprowicz M, Lalou DA, Czosnyka M, Garnett M, Czosnyka Z (2016). « Intracranial pressure, its components and cerebrospinal fluid pressure-volume compensation. » Acta Neurologica Scandinavica. 134(3):168–180. doi:10.1111/ane.12541.
- a, b, c, d, eVinje V, Ringstad G, Lindstrøm EK, Valnes LM, Rognes ME, Eide PK, et al. (2019). « Respiratory influence on cerebrospinal fluid flow—A computational study based on long-term intracranial pressure measurements. » Scientific Reports. 9(1):9732. doi:10.1038/s41598-019-46055-5.
- ^Dreha-Kulaczewski S, Joseph AA, Merboldt K-D, Ludwig H-C, Gärtner J, Frahm J (2017). « Identification of the Upward Movement of Human CSF In Vivo and its Relation to the Brain Venous System. » The Journal of Neuroscience. 37(9):2395–2402. doi:10.1523/JNEUROSCI.2754-16.2017.
- a, b, cGutiérrez-Montes C, Coenen W, Vidorreta M, Sincomb S, Martínez-Bazán C, Sánchez AL, et al. (2022). « Effect of Normal Breathing on the Movement of CSF in the Spinal Subarachnoid Space. » AJNR. American Journal of Neuroradiology. 43(9):1369–1374. doi:10.3174/ajnr.A7603.
- ^Mestre H, Tithof J, Du T, Song W, Peng W, Sweeney AM, et al. (2018). « Flow of cerebrospinal fluid is driven by arterial pulsations and is reduced in hypertension. » Nature Communications. 9(1):4878. doi:10.1038/s41467-018-07318-3.
- ^Budgell BS, Bolton PS (2007). « Cerebrospinal Fluid Pressure in the Anesthetized Rat. » Journal of Manipulative and Physiological Therapeutics. 30(5):351–356. doi:10.1016/j.jmpt.2007.04.002.
- ^Conductier G, Brau F, Viola A, Langlet F, Ramkumar N, Dehouck B, et al. (2013). « Melanin-concentrating hormone regulates beat frequency of ependymal cilia and ventricular volume. » Nature Neuroscience. 16(7):845–847. doi:10.1038/nn.3401.
- a, b, c, d, eWhedon JM, Glassey D (2009). « Cerebrospinal fluid stasis and its clinical significance. » Alternative Therapies in Health and Medicine. 15(3):54–60.
- a, bProulx ST (2021). « Cerebrospinal fluid outflow: A review of the historical and contemporary evidence for arachnoid villi, perineural routes, and dural lymphatics. » Cellular and Molecular Life Sciences: CMLS. 78(6):2429–2457. doi:10.1007/s00018-020-03706-5.
- a, bSakka L, Coll G, Chazal J (2011). « Anatomy and physiology of cerebrospinal fluid. » Annales françaises d’Oto-rhino-laryngologie et de Pathologie Cervico-faciale. 128(6):359–366. doi:10.1016/j.aforl.2011.09.004.
- ^Ligocki AP, Vinson AV, Yachnis AT, Dunn WA Jr, Smith DE, Scott EA, et al. (2024). « Cerebrospinal fluid flow extends to peripheral nerves further unifying the nervous system. » Science Advances. 10(36):eadn3259. doi:10.1126/sciadv.adn3259.
- a, bPessa JE (2022). « Ventricular Infusion and Nanoprobes Identify Cerebrospinal Fluid and Glymphatic Circulation in Human Nerves. » Plastic and Reconstructive Surgery. Global Open. 10(2):e4126. doi:10.1097/GOX.0000000000004126.
- a, bDreha-Kulaczewski S, Konopka M, Joseph AA, Kollmeier J, Merboldt K-D, Ludwig H-C, et al. (2018). « Respiration and the watershed of spinal CSF flow in humans. » Scientific Reports. 8(1):Article 1. doi:10.1038/s41598-018-23908-z.
- ^Weller RO (2005). « Microscopic morphology and histology of the human meninges. » Morphologie: Bulletin De l’Association Des Anatomistes. 89(284):22–34. doi:10.1016/s1286-0115(05)83235-7.
- ^Scapinelli R (1990). « Anatomical and radiologic studies on the lumbosacral meningo-vertebral ligaments of humans. » Journal of Spinal Disorders. 3(1):6–15.
- ^Wadhwani S, Loughenbury P, Soames R (2004). « The anterior dural (Hofmann) ligaments. » Spine. 29(6):623–627. doi:10.1097/01.brs.0000115129.59484.24.
- ^Wiltse LL, Fonseca AS, Amster J, Dimartino P, Ravessoud FA (1993). « Relationship of the dura, Hofmann’s ligaments, Batson’s plexus, and a fibrovascular membrane lying on the posterior surface of the vertebral bodies and attaching to the deep layer of the posterior longitudinal ligament. An anatomical, radiologic, and clinical study. » Spine. 18(8):1030–1043. doi:10.1097/00007632-199306150-00013.
- a, b, c, dBordoni B, Walkowski S, Ducoux B, Tobbi F (2020). « The Cranial Bowl in the New Millennium and Sutherland’s Legacy for Osteopathic Medicine: Part 2. » Cureus. 12(9). https://www.cureus.com/articles/40996-the-cranial-bowl-in-the-new-millennium-and-sutherlands-legacy-for-osteopathic-medicine-part-2.
- a, b, c, d, e, f, gAl-Habib A, Albakr A, Al Towim A, Alkubeyyer M, Abu Jamea A, Albadr F, et al. (2018). « In vivo assessment of spinal cord elasticity using shear wave ultrasound in dogs. » Journal of Neurosurgery. Spine. 29(4):461–469. doi:10.3171/2018.2.SPINE171195.
- a, b, c, dRoyo-Salvador MB, Solé-Llenas J, Doménech JM, González-Adrio R (2005). « Results of the section of the filum terminale in 20 patients with syringomyelia, scoliosis and Chiari malformation. » Acta Neurochirurgica. 147(5):515–523; discussion 523. doi:10.1007/s00701-005-0482-y.
- a, b, c, dRoyo-Salvador MB, Fiallos-Rivera MV, Salca HC, Ollé-Fortuny G (2020). « The Filum disease and the Neuro-Cranio-vertebral syndrome: Definition, clinical picture and imaging features. » BMC Neurology. 20:175. doi:10.1186/s12883-020-01743-y.
- a, b, cBordoni B, Zanier E (2015). « Sutherland’s legacy in the new millennium: The osteopathic cranial model and modern osteopathy. » Advances in Mind-Body Medicine. 29(2):15–21.
- ^Clayton EH, Genin GM, Bayly PV (2012). « Transmission, attenuation and reflection of shear waves in the human brain. » Journal of the Royal Society, Interface. 9(76):2899–2910. doi:10.1098/rsif.2012.0325.
- a, bHeisey SR, Adams T (1993). « Role of cranial bone mobility in cranial compliance. » Neurosurgery. 33(5):869–876; discussion 876-877. doi:10.1227/00006123-199311000-00014.
- ^King HH (2007). « The Inherent Rhythmic Motion of the Cranial Bones. » Cranial Letter. 60(1):7–10.
- a, bRetzlaff EW, Michael DK, Roppel RM (1975). « Cranial bone mobility. » The Journal of the American Osteopathic Association. 74(9):869–873.
- a, b, cSeimetz CN, Kemper AR, Duma SM (2012). « An investigation of cranial motion through a review of biomechanically based skull deformation literature. » International Journal of Osteopathic Medicine. 15(4):152–165. doi:10.1016/j.ijosm.2012.05.001.
- ^Rogers JS, Witt PL (1997). « The Controversy of Cranial Bone Motion. » Journal of Orthopaedic & Sports Physical Therapy. 26(2):95–103. doi:10.2519/jospt.1997.26.2.95.
- ^Khandare S, Bhise S, Shinde A (2015). « Age estimation from cranial sutures – a Postmortem study. » International Journal of Healh Care and Biomedical Research. 3–3.
- ^Todd T, Lyon D (1924). « Endocranial Suture Closure: Its Progress and Age Relationship. Part I. » Am. J. Phys. Anthropol. 7:325–384.
- ^Todd T, Lyon D (1925). « Cranial suture closure. Its progress and age relationship. Part III.—Endocranial closure in adult males of Negro stock. » Am. J. Phys. Anthropol. 8:47–71.
- a, bBassed RB, Briggs C, Drummer OH (2010). « Analysis of time of closure of the spheno-occipital synchondrosis using computed tomography. » Forensic Science International. 200(1–3):161–164. doi:10.1016/j.forsciint.2010.04.009.
- a, bStarkey R (2015). « Arguments for and against movement at the spheno-occipital synostosis: Furthering the debate. » International Journal of Osteopathic Medicine. 18(2):102–115. doi:10.1016/j.ijosm.2014.12.001.
- ^Madeline LA, Elster AD (1995). « Suture closure in the human chondrocranium: CT assessment. » Radiology. 196(3):747–756. doi:10.1148/radiology.196.3.7644639.
- ^Shirley NR, Jantz RL (2011). « Spheno-occipital synchondrosis fusion in modern Americans. » Journal of Forensic Sciences. 56(3):580–585. doi:10.1111/j.1556-4029.2011.01705.x.
- ^Downey PA, Barbano T, Kapur-Wadhwa R, Sciote JJ, Siegel MI, Mooney MP (2006). « Craniosacral Therapy: The Effects of Cranial Manipulation on Intracranial Pressure and Cranial Bone Movement. » Journal of Orthopaedic & Sports Physical Therapy. 36(11):845–853. doi:10.2519/jospt.2006.36.11.845.
- ^Dechant JJ, Mooney MP, Cooper GM, Smith TD, Burrows AM, Losken HW, et al. (1999). « Positional changes of the frontoparietal ossification centers in perinatal craniosynostotic rabbits. » Journal of Craniofacial Genetics and Developmental Biology. 19(2):64–74.
- ^Greenman PE, McPartland JM (1995). « Cranial findings and iatrogenesis from craniosacral manipulation in patients with traumatic brain syndrome. » JAOA: Journal of the American Osteopathic Association. 95(3):182–182.
- ^Oleski SL, Smith GH, Crow WT (2002). « Radiographic evidence of cranial bone mobility. » Cranio: The Journal of Craniomandibular Practice. 20(1):34–38. doi:10.1080/08869634.2002.11746188.
- ^Cook A (2005). « The mechanics of cranial motion—The sphenobasilar synchondrosis (SBS) revisited. » Journal of Bodywork and Movement Therapies. 9(3):177–188. doi:10.1016/j.jbmt.2004.12.002.
- ^Crow WT, King HH, Patterson RM, Giuliano V (2009). « Assessment of calvarial structure motion by MRI. » Osteopathic Medicine and Primary Care. 3(1):8. doi:10.1186/1750-4732-3-8.
- a, b, cGabutti M, Draper-Rodi J (2014). « Osteopathic decapitation: Why do we consider the head differently from the rest of the body? New perspectives for an evidence informed osteopathic approach to the head. » International Journal of Osteopathic Medicine. doi:10.1016/j.ijosm.2014.02.001.
- ^Herring SW, Teng S (2000). « Strain in the braincase and its sutures during function. » American Journal of Physical Anthropology. 112(4):575–593. doi:10.1002/1096-8644(200008)112:4<575::AID-AJPA10>3.0.CO;2-0.
- ^Jaslow CR (1990). « Mechanical properties of cranial sutures. » Journal of Biomechanics. 23(4):313–321. doi:10.1016/0021-9290(90)90059-C.
- ^Maloul A, Fialkov J, Whyne CM (2013). « Characterization of the bending strength of craniofacial sutures. » Journal of Biomechanics. 46(5):912–917. doi:10.1016/j.jbiomech.2012.12.016.
- ^Wang J-W, Yu K, Li M, Wu J, Wang J, Wan C-W, et al. (2022). « Application of nanoindentation technology in testing the mechanical properties of skull materials. » Scientific Reports. 12(1):8717. doi:10.1038/s41598-022-11216-6.
- ^Adams T, Heisey RS, Smith MC, Briner BJ (1992). « Parietal bone mobility in the anesthetized cat. » The Journal of the American Osteopathic Association. 92(5):599–600, 603–610, 615–622.
- a, b, cMoskalenko YE, Frymann V, Kravchenko T, Weinstein GB (2003). « Physiological Background of the Cranial Rhythmic Impulse and The Primary Respiratory Mechanism. » AAO Journal. 13(2):21–33.
- a, b, c, d, e, fHamm D (2011). « A hypothesis to explain the palpatory experience and therapeutic claims in the practice of osteopathy in the cranial field. » International Journal of Osteopathic Medicine. 14(4):149–165. doi:10.1016/j.ijosm.2011.07.003.
- ^Troup JDG (1986). « Biomechanics of the lumbar spinal canal. » Clinical Biomechanics. 1(1):31–43. doi:10.1016/0268-0033(86)90036-7.
- ^Dai LY, Xu YK, Zhang WM, Zhou ZH (1989). « The effect of flexion-extension motion of the lumbar spine on the capacity of the spinal canal. An experimental study. » Spine. 14(5):523–525.
- ^Cella M, Acella E, Aquino A, Pisa V (2022). « Cranial osteopathic techniques and electroencephalogram (EEG) alpha power: A controlled crossover trial. » Journal of Osteopathic Medicine. 122(8):401–409. doi:10.1515/jom-2021-0257.
- a, bMiana L, Hugo do Vale Bastos V, Machado S, Arias-Carrión O, Nardi AE, Almeida L, et al. (2013). « Changes in alpha band activity associated with application of the compression of fourth ventricular (CV-4) osteopathic procedure: A qEEG pilot study. » Journal of Bodywork and Movement Therapies. 17(3):291–296. doi:10.1016/j.jbmt.2012.10.002.
- a, bMoran RW, Gibbons P (2001). « Intraexaminer and interexaminer reliability for palpation of the cranial rhythmic impulse at the head and sacrum. » Journal of Manipulative and Physiological Therapeutics. 24(3):183–190. doi:10.1016/S0161-4754(01)62711-8.
- a, bRogers JS, Witt PL, Gross MT, Hacke JD, Genova PA (1998). « Simultaneous palpation of the craniosacral rate at the head and feet: Intrarater and interrater reliability and rate comparisons. » Physical Therapy. 78(11):1175–1185. doi:10.1093/ptj/78.11.1175.
- ^Jones TW (1853). « Discovery That the Veins of the Bat’s Wing (Which Are Furnished with Valves) Are Endowed with Rhythmical Contractility, and That the Onward Flow of Blood Is Accelerated by Such Contraction. » Edinburgh Medical and Surgical Journal. 79(195):367–373.
- ^Intaglietta M (1991). « Arteriolar vasomotion: Implications for tissue ischemia. » Blood Vessels. 28 Suppl 1:1–7. doi:10.1159/000158912.
- a, bMileva N, Velikova T, Velikov T, Vassilev D (2024). « Aortic Elasticity and Cardiovascular Risk Stratification: A Narrative Review on the Current Understanding. » Journal of Vascular Diseases. 3(1):88–101. doi:10.3390/jvd3010008.
- a, bFredriksson I, Larsson M, Strömberg T, Iredahl F (2021). « Vasomotion analysis of speed resolved perfusion, oxygen saturation, red blood cell tissue fraction, and vessel diameter: Novel microvascular perspectives. » Skin Research and Technology. 28(1):142–152. doi:10.1111/srt.13106.
- a, bStefanovska A, Bracic M, Kvernmo HD (1999). « Wavelet analysis of oscillations in the peripheral blood circulation measured by laser Doppler technique. » IEEE Transactions on Biomedical Engineering. 46(10):1230–1239. doi:10.1109/10.790500.
- ^Chaudhry R, Miao JH, Rehman A (2025). « Physiology, Cardiovascular. » In StatPearls. StatPearls Publishing. http://www.ncbi.nlm.nih.gov/books/NBK493197/.
- a, b, cPappano AJ, Gil Wier W (2013). « 9—The Peripheral Circulation and its Control. » In Pappano AJ, Gil Wier W (Eds.), Cardiovascular Physiology. 10th ed. Elsevier. pp. 171–194. doi:10.1016/B978-0-323-08697-4.00009-5.
- a, b, c, d, e, f, gNilsson H, Aalkjaer C (2003). « Vasomotion: Mechanisms and physiological importance. » Molecular Interventions. 3(2):79–89. doi:10.1124/mi.3.2.79.
- ^Peng H, Matchkov V, Ivarsen A, Aalkjaer C, Nilsson H (2001). « Hypothesis for the initiation of vasomotion. » Circulation Research. 88(8):810–815. doi:10.1161/hh0801.089603.
- a, bColantuoni A, Bertuglia S, Coppini G, Donato L (1990). « Superposition of arteriolar vasomotion waves and regulation of blood flow in skeletal muscle microcirculation. » Advances in Experimental Medicine and Biology. 277:549–558. doi:10.1007/978-1-4684-8181-5_62.
- a, bAon MA, Cortassa S, O’Rourke B (2008). « Mitochondrial Oscillations in Physiology and Pathophysiology. » Advances in Experimental Medicine and Biology. 641:98–117. doi:10.1007/978-0-387-09794-7_8.
- ^Cervera J, Meseguer S, Mafe S (2018). « Intercellular Connectivity and Multicellular Bioelectric Oscillations in Nonexcitable Cells: A Biophysical Model. » ACS Omega. 3(10):13567–13575. doi:10.1021/acsomega.8b01514.
- ^Figueroa XF, Duling BR (2009). « Gap Junctions in the Control of Vascular Function. » Antioxidants & Redox Signaling. 11(2):251–266. doi:10.1089/ars.2008.2117.
- ^Aalkjaer C, Nilsson H (2005). « Vasomotion: Cellular background for the oscillator and for the synchronization of smooth muscle cells. » British Journal of Pharmacology. 144(5):605–616. doi:10.1038/sj.bjp.0706084.
- a, bVillermain-Lecolier G, Billaudel P, Perrin E, Scherpereel B, Pire J-C (1994). « Detection of periodic micro movements using a non destructive method. » Rbm -Paris-. https://hal.science/hal-02334851.
- ^Billaudel P, Lecolier GV, Pire J, Laval Y (1991). « Detection of periodic micro movements of the head using a flat sensors system. » [1991 Proceedings] 6th Mediterranean Electrotechnical Conference. 752–755 vol.1. doi:10.1109/MELCON.1991.161947.
- 100.a, bStill AT (1897). Autobiography of Andrew T. Still, with a history of the discovery and development of the science of osteopathy, together with an account of the founding of the American school of osteopathy. Kirksville, Mo.: The author. http://archive.org/details/autobiographyand00stiliala.
- 101.^Barnett WH, Latash EM, Capps RA, Dick TE, Wehrwein EA, Molkov YI (2020). « Traube-Hering waves are formed by interaction of respiratory sinus arrhythmia and pulse pressure modulation in healthy men. » Journal of Applied Physiology. 129(5):1193–1202. doi:10.1152/japplphys.00452.2020.
- 102.a, b, c, dJulien C (2006). « The enigma of Mayer waves: Facts and models. » Cardiovascular Research. 70(1):12–21. doi:10.1016/j.cardiores.2005.11.008.
- 103.^Julien C (2008). « Baroreflex Control of Sympathetic Nerve Activity and Blood Pressure Variability. » Clinical and Experimental Pharmacology and Physiology. 35(4):512–515. doi:10.1111/j.1440-1681.2008.04907.x.
- 104.^deBoer R, Karemaker J, J S (1987). « Hemodynamic fluctuations and baroreflex sensitivity in humans: A beat-to-beat model. » The American Journal of Physiology. 253(3 Pt 2). doi:10.1152/ajpheart.1987.253.3.H680.
- 105.^La Fountaine M, Hohn A, Leahy C, Testa AJ, Weir JP (2022). « Use of Mayer wave activity to demonstrate aberrant cardiovascular autonomic control following sports concussion injury. » Annals of the New York Academy of Sciences. 1507(1). doi:10.1111/nyas.14683.
- 106.^Finucane C, Boyle G, Fan CW, Hade D, Byrne L, Kenny RA (2010). « Mayer wave activity in vasodepressor carotid sinus hypersensitivity. » Europace. 12(2):247–253. doi:10.1093/europace/eup385.
- 107.a, bJulien C (2019). « Physiology of low-frequency heart rate oscillations. » J. Physiol. 597(10):2595–2598. doi:10.1113/JP277500.
- 108.a, bGrasso R, Schena F, Gulli G, Cevese A (1997). « Does low-frequency variability of heart period reflect a specific parasympathetic mechanism? » Journal of the Autonomic Nervous System. 63(1):30–38. doi:10.1016/S0165-1838(96)00128-2.
- 109.^Fernandez D, Lecine A (1990). « Recording of the Traube-Hering wave and simultaneous cranial palpation. » Kinésithérapie scientifique. 292:33–40.
- ^Guinn K, Ali H, Seffinger M (2006). « Validation of Transcutaneous Laser Doppler Flowmeter in Measuring Autonomic Tone. » Journal of Investigative Medicine. 54(1):S172–S172. doi:10.2310/6650.2005.X0004.541.
- a, bChrist F, Raithel P, Gartside IB, Gamble J, Peter K, Messmer K (1995). « Investigating the origin of cyclic changes in limb volume using mercury-in-silastic strain gauge plethysmography in man. » The Journal of Physiology. 487(1):259–272. doi:10.1113/jphysiol.1995.sp020877.
- ^Baskin RJ, Paolini PJ (1966). « Muscle volume changes. » The Journal of General Physiology. 49(3):387–404. doi:10.1085/jgp.49.3.387.
- ^Scarr G (2016). « Fascial hierarchies and the relevance of crossed-helical arrangements of collagen to changes in shape; part II: The proposed effect of blood pressure (Traube-Hering-Mayer) waves on the fascia. » Journal of Bodywork and Movement Therapies. 20(3):629–638. doi:10.1016/j.jbmt.2015.10.008.
- ^Abenavoli A, Pisa S, Maggiani A (2020b). « A Pilot Study of Jugular Compression (Queckenstedt maneuver) for Cranial Movement Perception. » The Journal of the American Osteopathic Association. 120(10):647–654. doi:10.7556/jaoa.2020.119.
- a, b, cAbenavoli A, Badi F, Barbieri M, Bianchi M, Biglione G, Dealessi C, et al. (2020). « Cranial osteopathic treatment and stress-related effects on autonomic nervous system measured by salivary markers: A pilot study. » J Bodyw Mov Ther. 24(4):215–221. doi:10.1016/j.jbmt.2020.07.017.
- ^Taylor JA, Carr DL, Myers CW, Eckberg DL (1998). « Mechanisms underlying very-low-frequency RR-interval oscillations in humans. » Circulation. 98(6):547–555. doi:10.1161/01.cir.98.6.547.
- ^Cloarec-Blanchard L, Girard A, Houhou S, Grünfeld JP, Elghozi JL (1992). « Spectral analysis of short-term blood pressure and heart rate variability in uremic patients. » Kidney International. Supplement. 37:S14-18.
- ^Rajendra Acharya U, Paul Joseph K, Kannathal N, Lim CM, Suri JS (2006). « Heart rate variability: A review. » Medical & Biological Engineering & Computing. 44(12):1031–1051. doi:10.1007/s11517-006-0119-0.
- ^Stein PK, Bosner MS, Kleiger RE, Conger BM (1994). « Heart rate variability: A measure of cardiac autonomic tone. » American Heart Journal. 127(5):1376–1381. doi:10.1016/0002-8703(94)90059-0.
- 120.^Tiwari R, Kumar R, Malik S, Raj T, Kumar P (2021). « Analysis of Heart Rate Variability and Implication of Different Factors on Heart Rate Variability. » Current Cardiology Reviews. 17(5):e160721189770. doi:10.2174/1573403X16999201231203854.
- 121.^Pumprla J, Howorka K, Groves D, Chester M, Nolan J (2002). « Functional assessment of heart rate variability: Physiological basis and practical applications. » International Journal of Cardiology. 84(1):1–14. doi:10.1016/S0167-5273(02)00057-8.
- 122.^Ondicova K, Mravec B (2010). « Multilevel interactions between the sympathetic and parasympathetic nervous systems: A minireview. » Endocrine Regulations. 44(2):69–75. doi:10.4149/endo_2010_02_69.
- 123.a, b, c, d, eKeller M, Pelz H, Perlitz V, Zweerings J, Röcher E, Baqapuri HI, et al. (2020). « Neural correlates of fluctuations in the intermediate band for heart rate and respiration are related to interoceptive perception. » Psychophysiology. 57(9):e13594. doi:10.1111/psyp.13594.
- 124.a, bCarnevali L, Lombardi L, Fornari M, Sgoifo A (2020). « Exploring the Effects of Osteopathic Manipulative Treatment on Autonomic Function Through the Lens of Heart Rate Variability. » Frontiers in Neuroscience. 14:579365. doi:10.3389/fnins.2020.579365.
- 125.a, bPerlitz V, Lambertz M, Cotuk B, Grebe R, Vandenhouten R, Flatten G, et al. (2004). « Cardiovascular rhythms in the 0.15-Hz band: Common origin of identical phenomena in man and dog in the reticular formation of the brain stem? » Pflügers Archiv. 448(6):579–591. doi:10.1007/s00424-004-1291-4.
- 126.^Schwerdtfeger AR, Schwarz G, Pfurtscheller K, Thayer JF, Jarczok MN, Pfurtscheller G (2020). « Heart rate variability (HRV): From brain death to resonance breathing at 6 breaths per minute. » Clinical Neurophysiology: Official Journal of the International Federation of Clinical Neurophysiology. 131(3):676–693. doi:10.1016/j.clinph.2019.11.013.
- 127.^Keller M, Perlitz V, Pelz H, Borik S, Repik I, Geilgens A, et al. (2025). « Specificity of cranial cutaneous manipulations in modulating autonomic nervous system responses and physiological oscillations: A controlled study. » PloS One. 20(2):e0317300. doi:10.1371/journal.pone.0317300.
- 128.a, b, c, d, e, f, gNelson KE (2002). « The primary respiratory mechanism. » 12(4):25–34.
- 129.^Gretchin VB (1969). « Some data on oxygen dynamics in subcortical structures of the human brain. » Electroencephalography and Clinical Neurophysiology. 26(5):546–547.
- 130.^Kobayashi M, Musha T (1982). « 1/f fluctuation of heartbeat period. » IEEE Transactions on Bio-Medical Engineering. 29(6):456–457. doi:10.1109/TBME.1982.324972.
- 131.^Intaglietta M (1981). « Vasomotor activity, time-dependent fluid exchange and tissue pressure. » Microvascular Research. 21(2):153–164. doi:10.1016/0026-2862(81)90028-5.
- 132.a, bVern BA, Leheta BJ, Juel VC, LaGuardia J, Graupe P, Schuette WH (1998). « Slow oscillations of Cytochrome Oxidase Redox State and Blood Volume in Unanesthetized Cat and Rabbit Cortex. » Advances in Experimental Medicine and Biology. 454:561–570. doi:10.1007/978-1-4615-4863-8_67.
- 133.^Clark LC, Misrahy G, Fox RP (1958). « Chronically implanted polarographic electrodes. » J Appl Physiol. 13(1):85–91. doi:10.1152/jappl.1958.13.1.85.
- 134.^Steinmeier R, Bauhuf C, Hübner U, Bauer RD, Fahlbusch R, Laumer R, Bondar I (1996). « Slow rhythmic oscillations of blood pressure, intracranial pressure, microcirculation, and cerebral oxygenation. Dynamic interrelation and time course in humans. » Stroke. 27(12):2236–2243. doi:10.1161/01.str.27.12.2236.
- 135.^Breslin JW, Yang Y, Scallan JP, Sweat RS, Adderley SP, Murfee WL (2018). « Lymphatic Vessel Network Structure and Physiology. » Comprehensive Physiology. 9(1):207–299. doi:10.1002/cphy.c180015.
- 136.a, bMawhinney HJ, Roddie IC (1973). « Spontaneous activity in isolated bovine mesenteric lymphatics. » The Journal of Physiology. 229(2):339–348. doi:10.1113/jphysiol.1973.sp010141.
- 137.^McHale NG, Roddie IC (1976). « The effect of transmural pressure on pumping activity in isolated bovine lymphatic vessels. » The Journal of Physiology. 261(2):255–269.
- 138.^McGeown JG, McHale NG, Thornbury KD (1987). « The role of external compression and movement in lymph propulsion in the sheep hind limb. » The Journal of Physiology. 387:83–93. doi:10.1113/jphysiol.1987.sp016564.
- 139.^Hall JG, Morris B, Woolley G (1965). « Intrinsic rhythmic propulsion of lymph in the unanaesthetized sheep. » The Journal of Physiology. 180(2):336–349. doi:10.1113/jphysiol.1965.sp007706.
- 140.^Olszewski WL (2002). « Contractility patterns of normal and pathologically changed human lymphatics. » Annals of the New York Academy of Sciences. 979:52–63. doi:10.1111/j.1749-6632.2002.tb04867.x.
- 141.^Degenhardt BF, Kuchera ML (1996). « Update on osteopathic medical concepts and the lymphatic system. » The Journal of the American Osteopathic Association. 96(2):97–100. doi:10.7556/jaoa.1996.96.2.97.
- 142.^Kinmonth JB, Taylor GW, Tracy GD, Marsh JD (1957). « Primary lymphoedema; clinical and lymphangiographic studies of a series of 107 patients in which the lower limbs were affected. » The British Journal of Surgery. 45(189):1–9. doi:10.1002/bjs.18004518902.
- 143.a, bPerrin RN (2007). « Lymphatic Drainage of the Neuraxis in Chronic Fatigue Syndrome: A Hypothetical Model for the Cranial Rhythmic Impulse. » JAOA: Journal of the American Osteopathic Association. 107(6):218–224.
- 144.^Louveau A, Smirnov I, Keyes TJ, Eccles JD, Rouhani SJ, Peske JD, et al. (2015). « Structural and functional features of central nervous system lymphatic vessels. » Nature. 523(7560):337–341. doi:10.1038/nature14432.
- 145.^Bohr T, Hjorth PG, Holst SC, Hrabětová S, Kiviniemi V, Lilius T, et al. (2022). « The glymphatic system: Current understanding and modeling. » iScience. 25(9):104987. doi:10.1016/j.isci.2022.104987.
- 146.a, bPomerat CM (1959). « Rhythmic contraction of Schwann cells. » Science (New York, N.Y.). 130(3391):1759–1760. doi:10.1126/science.130.3391.1759-a.
- 147.a, bRetzlaff EW (1987). « Anatomy and Physiology of Craniosacral Mechanisms. » In Retzlaff EW, Mitchell FL (Eds.), The Cranium and Its Sutures: Anatomy, Physiology, Clinical Applications and Annotated Bibliography of Research in the Cranial Field. Springer. pp. 5–12. doi:10.1007/978-3-642-71848-9_2.
- 148.^Strumwasser F, Vogel JM (1992). « Cellular oscillators and biological timing: The role of proteins and Ca2+. » Progress in Brain Research. 92:309–320. doi:10.1016/s0079-6123(08)61185-1.
- 149.^Stecco A, Cowman M, Pirri N, Raghavan P, Pirri C (2022). « Densification: Hyaluronan Aggregation in Different Human Organs. » Bioengineering (Basel, Switzerland). 9(4):159. doi:10.3390/bioengineering9040159.
- 150.a, b, c, d, eMcPartland JM, Mein EA (1997). « Entrainment and the cranial rhythmic impulse. » Alternative Therapies in Health and Medicine. 3(1):40–45.
- 151.a, bNorton JM (1991). « A tissue pressure model for palpatory perception of the cranial rhythmic impulse. » JAOA: Journal of the American Osteopathic Association. 91(10):975–975.
- 152.a, b, c, dTiller WA, McCraty R, Atkinson M (1996). « Cardiac coherence: A new, noninvasive measure of autonomic nervous system order. » Alternative Therapies in Health and Medicine. 2(1):52–65.
- 153.^Greenman PE, Mein EA, Andary M (1996). « Craniosacral Manipulation. » Physical Medicine and Rehabilitation Clinics of North America. 7(4):877–896. doi:10.1016/S1047-9651(18)30371-1.
- 154.^Blechschmidt E (2004). The Ontogenetic Basis of Human Anatomy: A Biodynamic Approach to Development from Conception to Birth. North Atlantic Books.
- 155.^Blechschmidt E, Gasser R (2012). Biokinetics and Biodynamics of Human Differentiation: Principles and Applications. 2nd ed. North Atlantic Books.
- 156.a, bBecker RE (1997). Life in Motion. Portland, OR: Rudra Press.
- 157.^Rechberger V, Biberschick M, Porthun J (2019). « Effectiveness of an osteopathic treatment on the autonomic nervous system: A systematic review of the literature. » European Journal of Medical Research. 24(1):36. doi:10.1186/s40001-019-0394-5.
- 158.^Henley CE, Ivins D, Mills M, Wen FK, Benjamin BA (2008). « Osteopathic manipulative treatment and its relationship to autonomic nervous system activity as demonstrated by heart rate variability: A repeated measures study. » Osteopathic Medicine and Primary Care. 2:7. doi:10.1186/1750-4732-2-7.
- 159.^Tarsha MS, Park S, Tortora S (2019). « Body-Centered Interventions for Psychopathological Conditions: A Review. » Frontiers in Psychology. 10:2907. doi:10.3389/fpsyg.2019.02907.
- 160.^Milnes K, Moran RW (2007). « Physiological effects of a CV4 cranial osteopathic technique on autonomic nervous system function: A preliminary investigation. » International Journal of Osteopathic Medicine. 10(1):8–17. doi:10.1016/j.ijosm.2007.01.003.
- 161.^Nelson K, Sergueef N, Glonek T (2004). « Cranial manipulation induces sequential changes in blood flow velocity on demand. » AAO Journal. 14(3):15–17.
- 162.^Keller M, Perlitz V, Pelz H, Borik S, Repik I, Geilgens A, et al. (2024). On the specificity of manual triggers of autonomic nervous system responses using osteopathic cranial manipulative medicine. bioRxiv. https://doi.org/10.1101/2024.09.11.612567.
- 163.^Besson C, Mur T, Benaim C, Schmitt L, Gremeaux V (2023). « Short-term effects on heart rate variability of occipito-mastoid suture normalization in healthy subjects. » Frontiers in Neuroscience. 17:1271461. doi:10.3389/fnins.2023.1271461.
- 164.^Arienti C, Farinola F, Ratti S, Daccò S, Fasulo L (2020). « Variations of HRV and skin conductance reveal the influence of CV4 and Rib Raising techniques on autonomic balance: A randomized controlled clinical trial. » Journal of Bodywork and Movement Therapies. 24(4):395–401. doi:10.1016/j.jbmt.2020.07.002.
- 165.^Ruffini N, D’Alessandro G, Mariani N, Pollastrelli A, Cardinali L, Cerritelli F (2015). « Variations of high frequency parameter of heart rate variability following osteopathic manipulative treatment in healthy subjects compared to control group and sham therapy: Randomized controlled trial. » Frontiers in Neuroscience. 9:272. doi:10.3389/fnins.2015.00272.
- 166.^Fornari M, Carnevali L, Sgoifo A (2017). « Single Osteopathic Manipulative Therapy Session Dampens Acute Autonomic and Neuroendocrine Responses to Mental Stress in Healthy Male Participants. » The Journal of the American Osteopathic Association. 117(9):559–567. doi:10.7556/jaoa.2017.110.
- 167.^Bayo-Tallón V, Esquirol-Caussa J, Pàmias-Massana M, Planells-Keller K, Palao-Vidal DJ (2019). « Effects of manual cranial therapy on heart rate variability in children without associated disorders: Translation to clinical practice. » Complementary Therapies in Clinical Practice. 36:125–141. doi:10.1016/j.ctcp.2019.06.008.
- 168.^Byrne EA, Porges SW (1992). « Frequency-specific amplification of heart rate rhythms using oscillatory tilt. » Psychophysiology. 29(1):120–126. doi:10.1111/j.1469-8986.1992.tb02022.x.
- 169.^Tamburella F, Piras F, Piras F, Spanò B, Tramontano M, Gili T (2019). « Cerebral Perfusion Changes After Osteopathic Manipulative Treatment: A Randomized Manual Placebo-Controlled Trial. » Frontiers in Physiology. 10:403. doi:10.3389/fphys.2019.00403.
- 170.^Burch GE, Cohn AE, Neumann C (1942). « A study by quantitative methods of the spontaneous variations in volume of the finger tip, toe tip, and postero-superior portion of the pinna of resting normal white adults. » American Journal of Physiology-Legacy Content. 136(3):433–447. doi:10.1152/ajplegacy.1942.136.3.433.
- 171.^Dorko BL (2003). « The analgesia of movement: Ideomotor activity and manual care. » Journal of Osteopathic Medicine. 6(2):93–95. doi:10.1016/S1443-8461(03)80022-9.
- 172.^Spitz HH (1997). Nonconscious movements: From mystical messages to facilitated communication. Lawrence Erlbaum Associates, Inc. pp. xii, 202.
- 173.a, b, cShin YK, Proctor RW, Capaldi EJ (2010). « A review of contemporary ideomotor theory. » Psychological Bulletin. 136(6):943–974. doi:10.1037/a0020541.
- 174.^Pelz H, Keller M, Müller G, Mathiak K, Mayer J, Perlitz V (2022). « Immediate autonomic nervous system activity in skin microcirculation during osteopathic cranial vault hold intervention. » Research Square. doi:10.21203/rs.3.rs-2409912/v1.
- 175.^Barbaresi M, Nardo D, Fagioli S (2025). « Physiological Entrainment: A Key Mind–Body Mechanism for Cognitive, Motor and Affective Functioning, and Well-Being. » Brain Sciences. 15(1):3. doi:10.3390/brainsci15010003.
- 176.a, bBlacklaw-Jones RD (2009). « Comments on cranio-sacral method and efficacy. » International Journal of Osteopathic Medicine. 12(2):72–74. doi:10.1016/j.ijosm.2008.10.001.
- 177.^Mehling WE, Wrubel J, Daubenmier JJ, Price CJ, Kerr CE, Silow T, et al. (2011). « Body Awareness: A phenomenological inquiry into the common ground of mind-body therapies. » Philosophy, Ethics, and Humanities in Medicine: PEHM. 6:6. doi:10.1186/1747-5341-6-6.
- 178.^Tuladhar R, Bohara G, Grigolini P, West BJ (2018). « Meditation-Induced Coherence and Crucial Events. » Frontiers in Physiology. 9:626. doi:10.3389/fphys.2018.00626.
- 179.^Goshvarpour A, Goshvarpour A (2013). « Comparison of higher order spectra in heart rate signals during two techniques of meditation: Chi and Kundalini meditation. » Cognitive Neurodynamics. 7(1):39–46. doi:10.1007/s11571-012-9215-z.
- 180.^McCraty R (2022). « Following the Rhythm of the Heart: HeartMath Institute’s Path to HRV Biofeedback. » Applied Psychophysiology and Biofeedback. 47(4):305–316. doi:10.1007/s10484-022-09554-2.
- 181.^Kaur J, Fahmy LM, Davoodi-Bojd E, Zhang L, Ding G, Hu J, et al. (2021). « Waste Clearance in the Brain. » Frontiers in Neuroanatomy. 15. https://www.frontiersin.org/articles/10.3389/fnana.2021.665803.

